题目内容
9.实验室常用下列装置来制取氧气: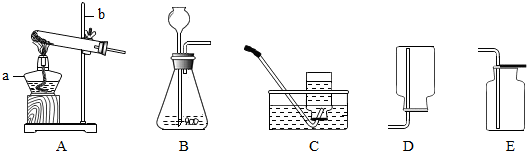
①写出图中有标号仪器的名称:a酒精灯、b铁架台;
②用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性.
Ⅰ.制取氨气反应的方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2X.X的化学式为:H2O.
Ⅱ.制取并收集NH3,应该从上图中选择的发生装置是A,收集装置是D.
Ⅲ.NH3是一种碱性气体,干燥时不能选用下列干燥剂中的B(填序号).
A.固体氢氧化钠 B.浓硫酸 C.生石灰.
分析 ①熟记仪器的名称;
②根据反应物的状态与反应条件确定制取装置,根据化学反应的原理来书写化学方程式;
③根据质量守恒定律分析X的化学式;根据实验室制取氨气的反应物状态、反应条件、氨气的性质可以选择发生装置和收集装置,根据氨气的性质来分析.
解答 解:①a是酒精灯;b是铁架台;故填:酒精灯;铁架台;
②双氧水是液体,二氧化锰是固体,也就是固液常温下的反应,所以选择装置B来制取氧气;过氧化氢在二氧化锰的催化作用下分解的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;故填:B;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③Ⅰ、制取氨气反应的方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2X.根据质量守恒定律可以知道反应前后原子的个数相等,反应物中所含的原子的种类和个数为:2N、10H、2Cl、Ca、2O,生成物中已知物质中原子的种类和个数为:Ca、2Cl、2N、6H,则两个X分子中含有4个氢原子和2个氧原子,一个X分子中含有2个氢原子和1个氧原子,X的化学式为H2O.故答案为:H2O;
Ⅱ、实验室制取氨气的反应物是固体,反应条件是加热,所以发生装置是A,氨气的密度比空气小,极易溶于水,所以收集装置是D;故填:A;D;
Ⅲ、干燥剂所干燥的气体必须不能与干燥剂发生反应,NH3是一种碱性气体,干燥时不能选用浓硫酸,因为浓硫酸能与氨气发生反应,故选B.
点评 本题主要考查化学方程式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、密度、能否和空气中的物质发生化学反应等因素.

| A. | FeCl3 | B. | CaCO3 | C. | CuSO4 | D. | Na2SO4 |
| A. | 酒精用作燃料--可燃性 | |
| B. | 石墨用作电极--质软 | |
| C. | 干冰用于人工降雨--密度比空气大 | |
| D. | 焦炭用于冶炼金属--碳单质的稳定性 |
| A. | N2、CO | B. | H2O (气)、N2 | C. | N2、CO2 | D. | HCI、CO |



