题目内容
4.走进高锰酸钾的世界(一)认识高锰酸钾
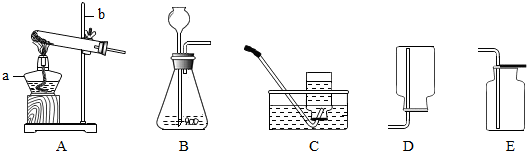
高锰酸钾,也叫PP粉,常温下为紫黑色(填颜色)片状固体,化学式KMnO4,易见光、受热易分解(写出文字表达式)高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,故需避光存于阴凉处.请从图1中选择高锰酸钾固体应储存在A(请填序号)试剂瓶中.

(二)粗略测定加热一定质量的高锰酸钾样品所收集到的氧气体积,并用制取的氧气,进行细铁丝在氧气中燃烧的性质实验.
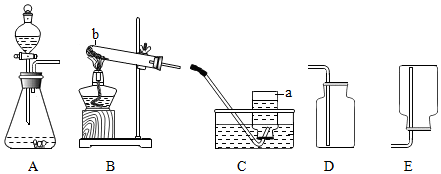
(1)仪器认识:写出图2仪器①②的名称:①试管;②量筒.
(2)反应原理:
铁丝在氧气中燃烧(文字表达式):铁+氧气$\stackrel{点燃}{→}$四氧化三铁,
实验现象:剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体.
(3)装置连接:图2中各装置的接口连接 a→c→b→f
(4)问题分析:
①在测量生成氧气体积的实验中,小组同学先加热图2A装置,将装置中空气排尽,然后正确连接各装置的接口.请判断这样操作是否合理:否(填“是”或“否”).实验结果发现,测得生成氧气的体积小于计算所得的数值.请写出导致实验结果误差的一点原因装置漏气.
②在进行细铁丝在氧气中燃烧的性质实验时,集气瓶发生破裂.请分析产生这一结果的可能原因集气瓶底部没有放少量的水或细沙(写出其中一点).
③小组同学经过调整实验步骤,经过严密的实验测定发现,收集到到氧气体积居然大于理论产量,并做出下列猜想,你认为他们的猜想可能正确的是B.
A.反应生成的二氧化锰分解放出氧气
B.反应生成的锰酸钾分解放出氧气
C.二氧化锰可能是锰酸钾分解的催化剂
D.装置漏气,空气中氧气混入制备得到的氧气中.
分析 (一)高锰酸钾是紫黑色片状固体,见光、受热易分解,所以要放在棕色试剂瓶中,避光保存保存;
(二)(1)根据实验室常见仪器的名称与用途填空;
(2)铁丝在氧气中燃烧,生成四氧化三铁,根据反应物、生成物以及反应条件书写反应方程式;
(3)装置连接:通过分析实验目的、气体的性质可以确定连接的顺序.
(4)①高锰酸钾受热会分解;制取气体前应先检查装置的气密性.
②做细铁丝在氧气中燃烧实验的注意事项.
③根据催化剂的特性进行判断.
解答 解:(一)高锰酸钾,常温下为紫黑色片状固体,其化学式为KMnO4,见光、受热易分解生成锰酸钾、二氧化锰和氧气,故需要存放于棕色试剂瓶内,避光保存.故答案是:紫黑色;KMnO4;高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;A;
(二)(1)①是试管;②是量筒;故答案是:试管;量筒;
(2)铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体.其反应的文字表达式为:铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
故答案是:铁+氧气$\stackrel{点燃}{→}$四氧化三铁;剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体;
(3)因为氧气的密度比水小,因此氧气应该从c进入来排出水,所以各装置的正确连接顺序是:acbf.
故答案是:c;b;
(4)①若先加热一会儿,一部分高锰酸钾受热分解生成的氧气扩散到空气中,会使收集到的氧气量不足;若装置漏气,一部分氧气会遗散到空气中,使收集到氧气的量偏小.故答案为:否;装置漏气;
②做细铁丝在氧气中燃烧实验时,应先在集气瓶底部放少量水或细沙,其目的是防止燃烧物溅落下来炸裂瓶底.
故答案为:集气瓶底部没有放少量的水或细沙.
③A、二氧化锰在该反应中起到催化作用,不影响生成物的质量,故A错误;
B、锰酸钾中含有氧元素,可能是锰酸钾被分解放出氧气,故B正确;
C、二氧化锰与锰酸钾均为高锰酸钾分解的产物,二氧化锰不可能做锰酸钾分解的催化剂,故C错误;
D、若装置漏气,一部分氧气会遗散到空气中,使收集到氧气的量偏小.故D错误.
故选:B.
点评 本题考查的是气体的制取装置和收集装置的选择、体积的测量,同时也考查了化学方程式的书写和实验探究的过程;气体的制取装置的选择与反应物的状态和反应的条件有关;收集装置的选择与气体的密度和溶解性有关.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 干冰用于人工降雨 | B. | 小苏打治疗胃酸过多 | ||
| C. | 稀硫酸用于金属除锈 | D. | 氦气常用作保护气 |
 小军用如图形式对所学知识进行归纳,其中甲包含乙、丙、丁…下列关系中,有错误的一组是( )
小军用如图形式对所学知识进行归纳,其中甲包含乙、丙、丁…下列关系中,有错误的一组是( )| 甲 | 乙、丙、丁… | |
| A | 盐 | 食盐、纯碱、高锰酸钾… |
| B | 合金 | 不锈钢、焊锡、生铁… |
| C | 溶液 | 碘酒、糖水、生理盐水… |
| D | 干燥剂 | 石灰石、浓硫酸、烧碱… |
| A. | A | B. | B | C. | C | D. | D |
| A. | Fe、Cu、Al2(SO4)3 溶液 | B. | Al、Cu、FeSO4 溶液 | ||
| C. | Fe、Al2(SO4)3溶液、CuSO4 溶液 | D. | Al、Fe、Cu、稀 H2SO4 |
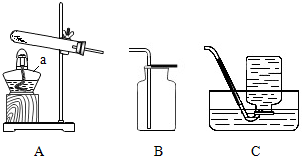
(1)仪器a的名称是酒精灯.
(2)实验室用高锰酸钾制取氧气的文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.用装置A、C制取氧气,收集完氧气时,应进行的操作是先将导管移出水面,再熄灭酒精灯.
(3)在老师指导下,同学们对一个化学反应可能有多种催化剂的问题进行了探究.
【提出猜想】除二气化锰(MnO2)外,氧化铜(CuO)、氧化铁(Fe2O3)也可以作氯酸钾(KClO3)
分解的催化剂.
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好).
| 实验编号 | 实验药品 | 分解温度/℃ |
| ① | KClO3 | 580 |
| ② | KClO3、MnO2(质量比1:1) | 350 |
| ③ | KClO3、CuO(质量比1:1) | 370 |
| ④ | KClO3、Fe2O3(质量比1:1) | 390 |
物质,催化效果最好的是二氧化锰.
【反思与拓展】若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质 不变; 同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证.
| 实验步骤 | 实验现象 | 实验结论 |
| 小颗粒的分解温度为380℃, 大颗粒的分解温度为390℃ |