题目内容
12.NaCl和Na2CO3的固体混合物与一定质量的稀盐酸恰好完全反应,得到4.4gCO2和100g21.1%的NaCl溶液,求:(1)稀盐酸中溶质的质量为7.3g.
(2)原混合物中NaCl的质量分数(写出计算过程).
分析 (1)根据生成CO2的质量,碳酸钠与稀HCl反应的化学方程式可以计算出原混合物中碳酸钠的质量、生成氯化钠的质量、氯化氢的质量.
(2)由生成氯化钠和所得液中氯化钠的质量可以计算出原混合物中NaCl的质量分数.
解答 解:设原混合物中Na2CO3的质量为x,生成NaCl的质量为y,氯化氢的质量为z
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x z y 4.4g
$\frac{106}{x}=\frac{73}{z}=\frac{117}{y}=\frac{44}{4.4g}$
x=10.6g,y=11.7g,z=7.3g
(2)原混合物中NaCl的质量;100g×21.1%-11.7g=9.4g
原混合物中NaCl的质量分数=$\frac{9.4g}{10.6g+9.4g}×100%$=47%
答:(1)7.3;
(2)原混合物中NaCl的质量分数为47%.
点评 本题主要考查含杂质物质的化学方程式计算和溶质质量分数的计算,难度较大.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
2.下列实验室中的交流,属于化学变化的是( )
| A. | 锥形瓶:“同学们不爱惜我,我被摔碎了” | |
| B. | 铁架台:“好难受啊!我在潮湿的空气中生锈了” | |
| C. | 酒精灯:“帽子哪里去了?我的燃料越来越少了” | |
| D. | 浓硫酸:“我在空气中放置一段时间质量怎么增加了” |
3.“舌尖上的中国”在央视上的热播让厨房再次成为人们施展厨艺的物态.大多数厨师有个工作经验:炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是醋中的乙酸与料酒只能怪的乙醇生成乙酸乙酯.如表中是几种常见的酯,请完成下列问题:
(1)甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为6:1:8;
(2)甲酸乙酯(C3H6O2)中碳元素的质量分数为48.6%(计算结果精确到0.1%);
(3)比较归纳是学习化学的重要方法,据表推测X额定化学式为C4H8O2.
| 酯的名称 | 甲酸甲酯 | 甲酸乙酯 | 乙酸甲酯 | 乙酸乙酯 |
| 化学式 | C2H4O2 | C3H6O2 | C3H6O2 | X |
(2)甲酸乙酯(C3H6O2)中碳元素的质量分数为48.6%(计算结果精确到0.1%);
(3)比较归纳是学习化学的重要方法,据表推测X额定化学式为C4H8O2.
20.如图所示实验操作,正确的是( )
| A. |  称量固体氢氧化钠 | B. |  测溶液pH | ||
| C. |  过滤 | D. |  稀释浓硫酸 |
4.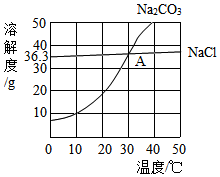 如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A.下列说法正确的是( )
如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A.下列说法正确的是( )
 如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A.下列说法正确的是( )
如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A.下列说法正确的是( )| A. | 碳酸钠俗称小苏打 | |
| B. | 30℃时,氯化钠的溶解度为36.3g | |
| C. | 碳酸钠的溶解度大于氯化钠的溶解度 | |
| D. | 将Na2CO3和NaCl均达到饱和的混合溶液,从40℃降温到20℃时,析出的固体物质主要是NaCl |
12.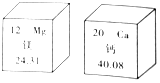 俗话说:“补钙不补镁,补了也后悔”,原来镁有协同钙的作用,会促进钙的吸收.如图是镁、钙在元素周期表中的部分信息,则下列说法不正确的是( )
俗话说:“补钙不补镁,补了也后悔”,原来镁有协同钙的作用,会促进钙的吸收.如图是镁、钙在元素周期表中的部分信息,则下列说法不正确的是( )
 俗话说:“补钙不补镁,补了也后悔”,原来镁有协同钙的作用,会促进钙的吸收.如图是镁、钙在元素周期表中的部分信息,则下列说法不正确的是( )
俗话说:“补钙不补镁,补了也后悔”,原来镁有协同钙的作用,会促进钙的吸收.如图是镁、钙在元素周期表中的部分信息,则下列说法不正确的是( )| A. | 镁和钙都属于金属元素 | B. | 在金属活动性顺序中,镁比钙活泼 | ||
| C. | 镁原子的质子数为12 | D. | 钙的相对原子质量为40.08 |
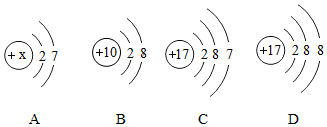 根据下图提供的信息,请回答下列问题:
根据下图提供的信息,请回答下列问题: