题目内容
13.矿物资源的综合利用,可以节约资源与能源.黄铁矿的主要成分为二硫化亚铁(FeS2),黄铁矿煅烧的化学方程式:4FeS2+11O2═2Fe2O3+8SO2.产生的SO2用于生产硫酸,矿渣(含有少量的硫元素)用于冶铁.查阅资料:SO2气体能使品红溶液褪色,能使澄清石灰水变浑浊,反应的化学方程式为SO2+Ca(OH)2═CaSO3↓+H2O.
(1)FeS2中硫元素的化合价为-1.矿渣在炼铁高炉内反应产生的高炉气含CO、CO2、SO2等气体,其中SO2是形成酸雨的气体.
(2)某化学兴趣小组为检验高炉气中的CO、CO2、SO2,设计了如图所示装置(不考虑其他气体对该实验的影响).

①该装置不能检验出的气体是CO2.
②装置B的作用是除去CO2、SO2.
③装置E中发生反应的化学方程式为CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2.
④确认高炉气中含CO的依据是bcd(填小写字母).
a.装置C中澄清石灰水变浑浊 b.装置C中澄清石灰水不变浑浊
c.装置E中黑色粉末变成红色 d.装置F中澄清石灰水变浑浊
(3)请指出该装置存在的一处明显缺陷没有处理尾气.
分析 (1)化合物中元素化合价代数和为零;
二氧化硫、氮氧化物是形成酸雨的重要物质;
(2)氢氧化钠能和二氧化碳反应生成碳酸钠和水,能和二氧化硫反应生成亚硫酸钠和水;
高温条件下,氧化铜和一氧化碳反应生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊;
(3)尾气中的一氧化碳有毒,扩散到空气中污染环境.
解答 解:(1)FeS2中铁元素化合价是+2,设硫元素的化合价为x,
根据题意有:(+2)×1+x×2=0,
x=-1,
矿渣在炼铁高炉内反应产生的高炉气含CO、CO2、SO2等气体,其中SO2是形成酸雨的气体.
故填:-1;SO2.
(2)①该装置不能检验出的气体是CO2,这是因为二氧化碳完全被B装置吸收.
故填:CO2.
②氢氧化钠能和二氧化碳反应生成碳酸钠和水,能和二氧化硫反应生成亚硫酸钠和水,因此装置B的作用是除去CO2、SO2.
故填:除去CO2、SO2.
③装置E中,氧化铜和一氧化碳反应生成铜和二氧化碳,发生反应的化学方程式为:CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2.
故填:CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2.
④确认高炉气中含CO的依据是:装置C中澄清石灰水不变浑浊,说明进入E装置的气体中不含有二氧化碳;
装置E中黑色粉末变成红色,说明氧化铜和一氧化碳发生了反应;
d.装置F中澄清石灰水变浑浊,说明氧化铜和一氧化碳反应生成了二氧化碳.
故选:bcd.
(3)该装置存在的一处明显缺陷是没有处理尾气.
故填:没有处理尾气.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
1.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而增大的是( )
| A. | 氯化钠溶液 | B. | 氢氧化钠溶液 | C. | 浓氨水 | D. | 浓硫酸 |
8.如图是四种粒子的结构示意图,对它们的描述正确的是( )

| A. | 四种粒子均表示原子 | B. | ②④两种粒子的电性相反 | ||
| C. | 四种粒子均达到了相对稳定结构 | D. | ①②两种粒子属于同一种元素 |
3.木糖醇是一种甜味剂,其溶解度曲线如图所示.下列关于木糖醇的叙述中不正确的是( )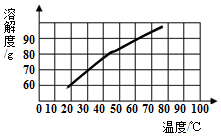

| A. | 木糖醇的溶解度随温度的升高而增大 | |
| B. | 木糖醇是易溶物质 | |
| C. | 70℃时木糖醇的饱和溶液降温到60℃会析出木糖醇晶体 | |
| D. | 50℃时,100g水中加入80g木糖醇,搅拌,可得到饱和溶液 |

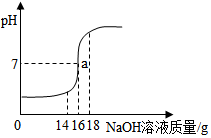 将10%的NaOH溶液逐滴加入到20克稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示,请计算:
将10%的NaOH溶液逐滴加入到20克稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示,请计算: