题目内容
有A、B、C三种无色溶液,所含的阴离子各不相同,进行如下实验:
①A溶液
白色沉淀
放出气体
变浑浊
B溶液
白色沉淀
沉淀不溶解
C溶液
白色沉淀
沉淀不溶解
②A溶液
大量气泡产生
请回答:
(1)A溶液中可能含有的阴离子是______.
(2)C溶液和BaCl2溶液反应生成的沉淀物是______.
(3)B溶液的pH______7(选填“>”或“<”或“=”),在B溶液中滴入紫色石蕊试液,可观察到溶液变色.
(4)B溶液与BaCl2溶液反应的化学方程式是______.
①A溶液
| BaCl 2溶液 |
| 稀硝酸 |
| 石灰水 |
B溶液
| BaCl 2溶液 |
| 稀硝酸 |
C溶液
| BaCl 2溶液 |
| 稀硝酸 |
②A溶液
| B溶液 |
请回答:
(1)A溶液中可能含有的阴离子是______.
(2)C溶液和BaCl2溶液反应生成的沉淀物是______.
(3)B溶液的pH______7(选填“>”或“<”或“=”),在B溶液中滴入紫色石蕊试液,可观察到溶液变色.
(4)B溶液与BaCl2溶液反应的化学方程式是______.
(1)根据①的实验现象,A溶液
白色沉淀
放出气体
变浑浊,推断出A溶液中一定含有
CO32-;A溶液中可能含有的阴离子是:Cl-、CO32-;故答案为:Cl-、CO32-;
(2)根据氯化银不溶于水也不溶于酸来检验氯离子方法,可推知C溶液和BaCl2溶液反应生成的沉淀物是:AgCl;
故答案为:AgCl;
(3)根据CO32-遇酸有气泡产生,推断B为H2SO4;由此可知B溶液的pH<7;故答案为:<;
(4)根据书写化学方程式的步骤写、配、注、等,B溶液与BaCl2溶液反应的化学方程式为:H2SO4+BaCl2=BaSO4↓+2HCl 故答案为:H2SO4+BaCl2=BaSO4↓+2HCl.
| BaCl 2溶液 |
| 稀硝酸 |
| 石灰水 |
CO32-;A溶液中可能含有的阴离子是:Cl-、CO32-;故答案为:Cl-、CO32-;
(2)根据氯化银不溶于水也不溶于酸来检验氯离子方法,可推知C溶液和BaCl2溶液反应生成的沉淀物是:AgCl;
故答案为:AgCl;
(3)根据CO32-遇酸有气泡产生,推断B为H2SO4;由此可知B溶液的pH<7;故答案为:<;
(4)根据书写化学方程式的步骤写、配、注、等,B溶液与BaCl2溶液反应的化学方程式为:H2SO4+BaCl2=BaSO4↓+2HCl 故答案为:H2SO4+BaCl2=BaSO4↓+2HCl.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
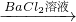 白色沉淀
白色沉淀 放出气体
放出气体 变浑浊
变浑浊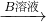 大量气泡产生
大量气泡产生