题目内容
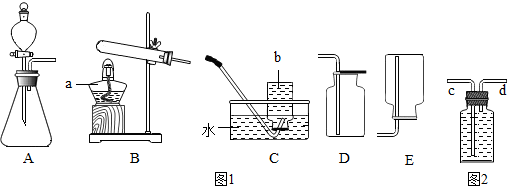
12.如图1装置适当组合可用于O2、H2、CO2等气体的制备和收集.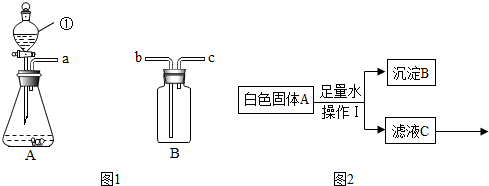
(1)仪器①的名称是分液漏斗,若A装置内药品为MnO2和过氧化氢溶液,反应的方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.若A装置内药品为Zn和稀盐酸,反应的方程式为Zn+2HCl=ZnCl2+H2↑.
(2)B装置正放桌面,用于收集A生成的O2,则a接b(选填“b”或“c”);若B装满水,用于收集A生成的H2,则a接c(选填“b”或“c”).
(3)如果要制取和收集干燥的CO2,需要在A装置之后连接两个B装置,则在前一个B装置内加入的试剂是浓硫酸(选填“浓硫酸”或“氢氧化钠”).
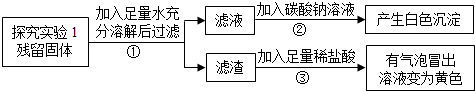
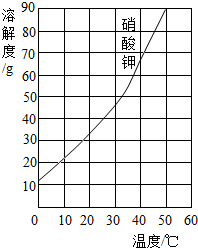
(4)某白色固体A可能含有碳酸钠、氯化钡(水溶液呈中性),氢氧化钠中的一种或几种,进行如图2实验.
完成下列填空:
①操作Ⅰ是过滤,根绝上述实验分析,A中一定含有的物质是碳酸钠、氯化钡,C中一定含有的溶质是氯化钠.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表.
| 实验操作 | 现象 | 结论 |
| 向滤液C中加入过量的氯化钡溶液,充分反应后,静置,取上层清液滴加无色酚酞试液 | 无色变红色 | A中有氢氧化钠 |
分析 分液漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.B装置正放桌面,用于收集A生成的O2,则a接长管,因为氧气的密度比空气大;若B装满水,用于收集A生成的H2,则a接短管,因为氢气的密度比水小.操作Ⅰ是过滤,根绝图中的实验分析,A中一定含有的物质是碳酸钠、氯化钡,因为碳酸钠与氯化钡反应生成碳酸钡白色沉淀和氯化钠;C中一定含有的溶质是氯化钠,因为氯化钠是生成物.为进一步确定固体A中可能存在的物质,对滤液C进行实验:向滤液C中加入过量的氯化钡溶液,充分反应后,静置,取上层清液滴加无色酚酞试液,无色变红色,证明A中有氢氧化钠.
解答 解:(1)分液漏斗方便加液体药品,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,锌和盐酸反应生成氯化锌和氢气,要注意配平;故答案为:分液漏斗;2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑;Zn+2HCl=ZnCl2+H2↑;
(2)B装置正放桌面,用于收集A生成的O2,则a接长管,因为氧气的密度比空气大;若B装满水,用于收集A生成的H2,则a接短管,因为氢气的密度比水小;故答案为:b;c;
(3)二氧化碳可以用浓硫酸干燥,故答案为:浓硫酸;
(4)操作Ⅰ是过滤,根绝图中的实验分析,A中一定含有的物质是碳酸钠、氯化钡,因为碳酸钠与氯化钡反应生成碳酸钡白色沉淀和氯化钠;C中一定含有的溶质是氯化钠,因为氯化钠是生成物;为进一步确定固体A中可能存在的物质,对滤液C进行实验:向滤液C中加入过量的氯化钡溶液,充分反应后,静置,取上层清液滴加无色酚酞试液,无色变红色,证明A中有氢氧化钠;故答案为:①过滤;碳酸钠、氯化钡;氯化钠;②向滤液C中加入过量的氯化钡溶液,充分反应后,静置,取上层清液滴加无色酚酞试液;无色变红色;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和物质的推断等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案| A. | 乳酸是由碳元素、氢元素、氧元素组成的 | |
| B. | 乳酸的相对分子质量为90 | |
| C. | 乳酸中碳元素与氢元素的质量比为1:2 | |
| D. | 乳酸中碳元素的质量分数为40% |
| A. | 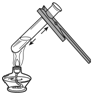 给液体加热 | B. | 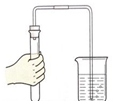 检查装置气密性 | ||
| C. |  取粉末状固体颗粒 | D. |  加热胆矾固体 |
| A. | 等于4.0% | B. | 大于4.0%,小于6.0% | ||
| C. | 等于6.0% | D. | 大于6.0% |
| A. | 烧杯、玻璃棒 | B. | 大试管、集气瓶 | C. | 导管、单孔塞 | D. | 酒精灯、铁架台 |
 无土栽培是现代农业栽培植物的一种方法.无土栽培的植物从营养液中吸取养料和水分.
无土栽培是现代农业栽培植物的一种方法.无土栽培的植物从营养液中吸取养料和水分.