题目内容
12. 某同学用如图所示的装置制取氧气并实验证氧气的性质
某同学用如图所示的装置制取氧气并实验证氧气的性质(1)指出装置中的错误:
a不能加热
b伸入锥形瓶的导管过长
c长颈漏斗的末端没有伸入液面以下
(2)写出标有序号仪器名称:③长颈漏斗④水槽
(3)图中是用排水法收集氧气,用这种方法收集氧气的原因是氧气不易溶于水,还可以用向上排空气法收集氧气,用此方法收集,怎样检验集气瓶中氧气已收集满了?将一根带火星的木条放在集气瓶口,若木条复燃,证明氧气已满,收集满氧气的集气瓶应正放在桌子上,原因是氧气的密度比空气大.
(4)某同学用如图所示方法收集氧气很长时间不满,出现这种情况的原因可能有装置漏气或药品不足.
(5)实验室用过氧化氢溶液和二氧化锰制取氧气大致可分为下列步骤:①向锥形瓶中加入二氧化锰固体粉末,用带有导管的塞子塞紧瓶口;②检查装置的气密性;③用排水法收集氧气;④向长颈漏斗中倒入过氧化氢溶液;⑤组装仪器装置;正确的操作顺序是⑤②①④③
(6)写出实验室用过氧化氢溶液和二氧化锰制取氧气反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应基本类型是分解反应,此反应中二氧化锰起催化作用.
分析 (1)根据实验室中用双氧水制取氧气的注意事项来分析;
(2)要熟悉常见化学实验仪器;
(3)根据氧气的性质来分析收集方法和验满以及放置方法;
(4)利用收集不到气体的可能原因解答;
(5)根据实验室用双氧水制取氧气的步骤进行解答;
(6)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;再根据反应特征确定反应类型.
解答 解:(1)在实验室中,用过氧化氢溶液分解制取氧气是在常温下进行的,不能加热;伸入锥形瓶的导管不能太长,这样不利于氧气的导出;长颈漏斗的末端要伸入液面以下,以防氧气由长颈漏斗逸出;
故填:(2)①是长颈漏斗,②是锥形瓶,③是导管,④是水槽;
(3)图中是用排水法收集氧气,因为氧气不易溶于水,又因为氧气的密度比空气大,还可以用向上排空气法收集氧气,用此方法收集,可将一根带火星的木条放在集气瓶口,观察是否复燃来进行集气瓶中氧气已收集满了;因为氧气的密度比空气大,所以收集满氧气的集气瓶应正放在桌子上.
(4)集气瓶中氧气若长时间收集不满,请分析其原因可能是:装置漏气、药品不足等;故答案:装置漏气;药品不足;
(5)实验室用双氧水制取氧气一般有以下几个步骤:检查装置的气密性;向锥形瓶中加入少量二氧化锰;塞好带有长颈漏斗和导管的双孔塞;向长颈漏斗中加入过氧化氢溶液;用排水法收集气体.故填:⑤②①④③;
(6)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;该反应符合“一变多”的特征,属于分解反应.其中二氧化锰加快了过氧化氢的分解速率,起到了催化作用;
答案:(1)不能加热;伸入锥形瓶的导管过长;长颈漏斗的末端没有伸入液面以下;
(2)③长颈漏斗;④水槽;
(3)排水;氧气不易溶于水;向上排空气;将一根带火星的木条放在集气瓶口,若木条复燃,证明氧气已满;正;氧气的密度比空气大;
(4)装置漏气;药品不足;
(5)⑤②①④③;
(6)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;分解反应;催化
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 用火柴点燃酒精灯 | B. | 酒精着火,用湿抹布扑盖 | ||
| C. | 用酒精灯外焰给物质加热 | D. | 熄灭酒精灯用嘴吹灭 |
| A. |  收集氧气 收集氧气 | B. |  收集氧气 | C. |  氧气的验满 | D. |  加热高锰酸钾 加热高锰酸钾 |
| A. | N2 | B. | H2 | C. | O2 | D. | Hg |
| A. | 4:5 | B. | 5:6 | C. | 6:5 | D. | 5:4 |
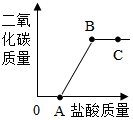 取实验室中部分变质的NaOH样品配成溶液,向其中滴加稀盐酸,绘制出生成的CO2的质量与加入的盐酸的质量关系如图所示,下列有关说法正确的是( )
取实验室中部分变质的NaOH样品配成溶液,向其中滴加稀盐酸,绘制出生成的CO2的质量与加入的盐酸的质量关系如图所示,下列有关说法正确的是( )| A. | OA段没有发生任何化学反应 | |
| B. | A点溶液中的溶质只有NaCl | |
| C. | C点的溶液的pH=7 | |
| D. | B点表示加入的盐酸与原溶液中的溶质恰好完全反应 |
| A. |  过滤 | B. |  塞紧橡胶塞 | ||
| C. |  向试管中加入固体 | D. |  用滴管滴加液体 |
