题目内容
10.下列关于除去粗盐中的泥沙的操作中错误的是( )| A. |  称量 | B. |  溶解 | C. |  过滤 | D. |  蒸发 |
分析 A、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断.
B、根据溶解操作的方法,进行分析判断.
C、过滤液体时,注意“一贴、二低、三靠”的原则.
D、根据蒸发操作的注意事项进行分析判断.
解答 解:A、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图中所示操作正确.
B、溶解时,应用玻璃棒进行搅拌,图中所示操作正确.
C、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,图中所示操作错误.
D、蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造成液体飞溅,图中所示操作正确.
故选:C.
点评 本题难度不大,熟悉粗盐提纯的实验步骤、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
20.某同学要探究燃烧的条件和空气中氧气的含量,进行了如下实验.
【实验一】(已知:白磷的着火点为40℃)
(1)对比步骤Ⅱ和Ⅳ的现象可知,可燃物燃烧的条件之一是温度达到着火点
(2)待装置冷却一段时间后,打开K2,如果观察到水倒流进A瓶40mL,说明空气中氧气的体积约占$\frac{1}{5}$.若实验测得空气中氧气的体积分数小于$\frac{1}{5}$,原因可能是气密性不好、未等装置冷却就打开夹子等(答一条即可).
【实验二】用如图所示装置,利用铁生锈的原理也可以比较准确地测出空气中氧气的含量.若将此装置中的细铁丝换成足量的细铜丝进行实验,能否比较准确地测出空气中氧气的含量,并说明理由不能;因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.【已知:铜能与空气中氧气、水、二氧化碳反应生成铜绿.化学方程式:2Cu+O2+H2O+CO2═Cu(OH)2CO3】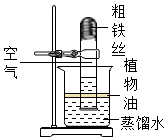
【实验一】(已知:白磷的着火点为40℃)
| 实验装置 | 实验步骤及现象 |
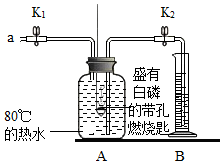 | 步骤Ⅰ.检验装置的气密性,气密性良好. 步骤Ⅱ.将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧. 步骤Ⅲ.向A瓶中加满80℃热水,塞紧瓶塞,白磷不燃烧. 步骤Ⅳ.打开K1、K2,从a口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2.此时进入量筒B中水的体积为200mL,观察到A瓶中的白磷燃烧. |
(2)待装置冷却一段时间后,打开K2,如果观察到水倒流进A瓶40mL,说明空气中氧气的体积约占$\frac{1}{5}$.若实验测得空气中氧气的体积分数小于$\frac{1}{5}$,原因可能是气密性不好、未等装置冷却就打开夹子等(答一条即可).
【实验二】用如图所示装置,利用铁生锈的原理也可以比较准确地测出空气中氧气的含量.若将此装置中的细铁丝换成足量的细铜丝进行实验,能否比较准确地测出空气中氧气的含量,并说明理由不能;因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.【已知:铜能与空气中氧气、水、二氧化碳反应生成铜绿.化学方程式:2Cu+O2+H2O+CO2═Cu(OH)2CO3】

5.甲、乙、丙、丁四种物质的转化关系如图所示.下列说法正确的是( )


| A. | 若丙为气体,则甲、乙中一定有单质 | |
| B. | 若丙为沉淀,则甲、乙中一定有一种物质是碱 | |
| C. | 若丁为水,则该反应不一定是中和反应 | |
| D. | 若甲、乙、丙、丁为化合物,则该反应一定是复分解反应 |
2. 2017年5月18日,我国全球首次海域试采可燃冰获得成功.可燃冰(CH4•xH2O)晶体中平均每46个水分子构成8个笼,每个笼可容纳1个CH4分子或1个H2O分子,每8个笼中有6个容纳CH4分子,2个笼填充H2O分子.下列说法中正确的是( )
2017年5月18日,我国全球首次海域试采可燃冰获得成功.可燃冰(CH4•xH2O)晶体中平均每46个水分子构成8个笼,每个笼可容纳1个CH4分子或1个H2O分子,每8个笼中有6个容纳CH4分子,2个笼填充H2O分子.下列说法中正确的是( )
 2017年5月18日,我国全球首次海域试采可燃冰获得成功.可燃冰(CH4•xH2O)晶体中平均每46个水分子构成8个笼,每个笼可容纳1个CH4分子或1个H2O分子,每8个笼中有6个容纳CH4分子,2个笼填充H2O分子.下列说法中正确的是( )
2017年5月18日,我国全球首次海域试采可燃冰获得成功.可燃冰(CH4•xH2O)晶体中平均每46个水分子构成8个笼,每个笼可容纳1个CH4分子或1个H2O分子,每8个笼中有6个容纳CH4分子,2个笼填充H2O分子.下列说法中正确的是( )| A. | 可燃冰是一种洁净的化石燃料,属于可再生能源 | |
| B. | 可燃冰的平均组成可表示为CH4•8H2O | |
| C. | 可燃冰完全燃烧时反应方程式:CH4•xH2O+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2xH2O | |
| D. | 可燃冰燃烧实现了热能转化为化学能 |
19.兴奋剂检测是奥运会对运动员的一项重要检验.某种兴奋剂的化学式为C20H26O2,则下列关于该兴奋剂的说法正确的是( )
| A. | 该兴奋剂是由原子直接构成的 | |
| B. | 该兴奋剂是由碳、氢、氧三个元素组成的 | |
| C. | 该兴奋剂属于有机化合物 | |
| D. | 该兴奋剂中碳、氢、氧三种元素的质量比为10:13:1 |
 炎热的夏季是“登革热(dengue fever)”的高发期,防止蚊虫滋生、预防蚊虫叮咬成为预防“登革热”的重要手段.蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.蚁酸化学名称叫甲酸,化学式为HCOOH.
炎热的夏季是“登革热(dengue fever)”的高发期,防止蚊虫滋生、预防蚊虫叮咬成为预防“登革热”的重要手段.蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.蚁酸化学名称叫甲酸,化学式为HCOOH.
 老师在第十单元课题2“酸和碱的中和反应”课堂演示了酸碱中和滴定实验,但对实验进行了改进,并对两个问题进行了讨论.
老师在第十单元课题2“酸和碱的中和反应”课堂演示了酸碱中和滴定实验,但对实验进行了改进,并对两个问题进行了讨论.