题目内容
将6.4g氧化铁与适量的碳粉混合均匀后,装入试管加强热,使其完全反应,反应后试管里剩余的固体的质量是多少?(用两种方法计算)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:氧化铁与碳粉在高温下反应生成铁和二氧化碳,由常见反应的氧化铁的质量利用反应的化学方程式计算出反应后试管里剩余的固体的质量即可.
或由质量守恒定律,反应前后元素的质量不变,反应后试管里剩余的固体为铁,氧化铁中铁元素的质量即为试管里剩余的固体的质量.
或由质量守恒定律,反应前后元素的质量不变,反应后试管里剩余的固体为铁,氧化铁中铁元素的质量即为试管里剩余的固体的质量.
解答:解:设反应后试管里剩余的固体的质量是x
3C+2Fe2O3
4Fe+3CO2↑
320 224
6.4g x
=
x=4.48g
或由质量守恒定律,反应前后元素的质量不变,反应后试管里剩余的固体为铁,氧化铁中铁元素的质量即为试管里剩余的固体的质量.6.4g氧化铁6.4g×
×100%=4.48g.
答:反应后试管里剩余的固体的质量是4.48g.
3C+2Fe2O3
| ||
320 224
6.4g x
| 320 |
| 224 |
| 6.4g |
| x |
或由质量守恒定律,反应前后元素的质量不变,反应后试管里剩余的固体为铁,氧化铁中铁元素的质量即为试管里剩余的固体的质量.6.4g氧化铁6.4g×
| 56×2 |
| 56×2+16×3 |
答:反应后试管里剩余的固体的质量是4.48g.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
下列实验现象描述不正确的是( )
| A、细铁丝在氧气里剧烈燃烧,火星四射 |
| B、一氧化碳燃烧产生蓝色火焰 |
| C、硫在空气中燃烧产生蓝紫色火焰 |
| D、白磷在空气中自燃产生大量白烟 |
有人设计下列实验步骤,用食盐固体配制50g 5%的食盐溶液,其中不必要的是( )
| A、计算,确定所需食盐和水的质量 |
| B、称量,按计算结果称取食盐,量取水 |
| C、溶解,将称好的食盐溶解于水中 |
| D、验算,计算所配溶液的溶质质量分数 |
下列实验操作符合操作规范的是( )
| A、为了便于观察,给试管加热时,试管口应对着自己 |
| B、为了证明一瓶药品是蔗糖还是食盐,可品尝一下其味道 |
| C、实验室用剩的药品,不能放回原瓶,但可丢入垃圾堆中 |
| D、熄灭酒精灯时用灯帽盖灭 |
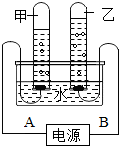 测定水的组成实验装置,根据观察到的实验现象回答:
测定水的组成实验装置,根据观察到的实验现象回答: