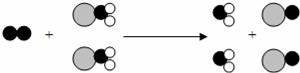题目内容
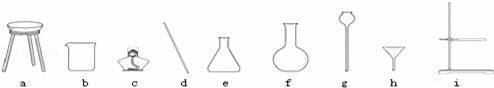
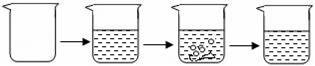
根据如图所示回答问题.
(1)图中a仪器的名称为 .
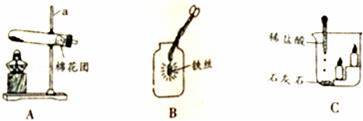
(2)A装置可用于制取氧气,反应的化学方程式为 ,在该实验中棉花团的作用是 .将收集到的氧气用来做铁丝燃烧的实验,如装置B,但该装置存在缺陷,你改进的措施是
(3)滴加稀盐酸后,C实验中,观察到燃着的蜡烛发生的现象是 ,此实验说明CO2具有的性质是 .

【考点】氧气的制取装置;氧气的化学性质;制取氧气的操作步骤和注意点;二氧化碳的物理性质;二氧化碳的化学性质;书写化学方程式、文字表达式、电离方程式.
【专题】实验性简答题.
【分析】(1)熟记仪器的名称;
(2)据A装置是加热固体制取氧气,且试管口有棉花可知是用加热高锰酸钾的方法制取氧气,并据反应原理书写方程式,据反应特点和注意事项解答;
(3)二氧化碳的密度比空气大,不能燃烧也不能支持燃烧,可以据此解答该题.
【解答】解:(1)a仪器是铁架台;故填:铁架台;
(2)A装置是加热固体制取氧气,且试管口有棉花可知是用加热高锰酸钾的方法制取氧气,反应的化学方程式为:2KMnO4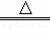
 K2MnO4+MnO2+O2↑,加热时在试管口放棉花是为了防止加热时高锰酸钾粉末进入导管;做铁丝在氧气中的燃烧实验时,为了防止高温生成物溅落炸裂瓶底,所以需要瓶底放少量的水或铺一层细砂.故填:
K2MnO4+MnO2+O2↑,加热时在试管口放棉花是为了防止加热时高锰酸钾粉末进入导管;做铁丝在氧气中的燃烧实验时,为了防止高温生成物溅落炸裂瓶底,所以需要瓶底放少量的水或铺一层细砂.故填:
2KMnO4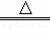
 K2MnO4+MnO2+O2↑,防止加热时高锰酸钾粉末进入导管,实验前集气瓶底应预先留有少量的水或铺上一层细沙;
K2MnO4+MnO2+O2↑,防止加热时高锰酸钾粉末进入导管,实验前集气瓶底应预先留有少量的水或铺上一层细沙;
(3)稀盐酸与石灰石反应生成了二氧化碳,由于二氧化碳的密度比空气大,不能燃烧也不能支持燃烧,所以可以观察到C中的蜡烛自下而上依次熄灭.故填:蜡烛自下而上依次熄灭;二氧化碳的密度比空气大,不能燃烧也不能支持燃烧.
【点评】该题为实验室制取氧气和二氧化碳的一道综合题,考查二氧化碳的实验室制法原理、制取装置、收集装置的选择,以及二氧化碳的某些性质.

“化学反应条件的控制是实验的灵魂”.某探究小组发现若反应过快,产生的气体不易及时收集,为探究影响过氧化氢溶液分解快慢的因素,于是进行了如下探究:
【提出问题】过氧化氢溶液分解快慢与哪些因素有关呢?
【猜想与假设】猜想一:可能与过氧化氢的质量分数有关;
猜想二:可能与 有关;
猜想三:可能与是否用催化剂有关.
【设计并实验】该探究小组用不同质量分数的过氧化氢溶液在不同温度时进行四次实验.记录所生成的氧气体积和反应所需时间,记录数据如表.
| 实验 序号 | 过氧化氢的 质量分数 | 过氧化氢溶液 体积(mL) | 温度 | 二氧化锰 的用量/g | 收集氧气 的体积/ml | 反应所需 的时间/s |
| ① | 5% | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15% | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30% | 5 | 35 | 2 | 49.21 | |
| ④ | 30% | 5 | 55 | 2 | 10.76 |
【收集证据】要比较不同质量分数的过氧化氢溶液对反应快慢的影响,应选择的实验编号组合是
(选填“实验序号”).由实验③和④对比可知,化学反应速率与温度的关系是: .
【解释与结论】
(1)通过探究,了解控制过氧化氢分解快慢的方法.请写出过氧化氢溶液在二氧化锰的催化作用下生成氧气的化学方程式为: .
(2)用一定量15%的过氧化氢溶液制氧气,为了减缓反应速率,可加适量的水稀释,所产生氧气的总质量 .(填“减小”、“增大”或“不变”)
石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
| 实验步骤 | ①称取烧杯的质量 | ②将适量盐酸加入烧杯中并称重 | ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验图示 |
| |||
| 实验数据 | 烧杯的质量为50.0g | 烧杯和盐酸的质量为100.0g | 石灰石样品样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水)

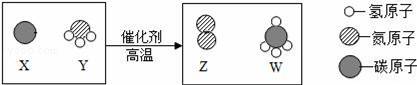


 表示氧原子,
表示氧原子,
 表示钠原子,
表示钠原子,
 表示氯原子),依据上述信息可知,下列说法中正确的是( )
表示氯原子),依据上述信息可知,下列说法中正确的是( )