题目内容
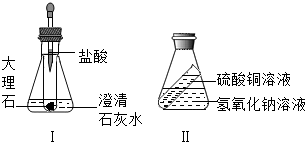
某同学利用“多米诺骨牌“效应,设计了如下气体制取与性质验证的组合实验.打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色.请看图回答问题:

(1)A中反应的化学方程式 ;B中白磷不燃烧,原因是 .
(2)C、D中看到的现象分别是 、 ;写出D中发生反应的化学方程式 .
(3)用化学方程式表示E中颜色变化的原因 .
(4)用F装置收集气体的依据是 .

(1)A中反应的化学方程式
(2)C、D中看到的现象分别是
(3)用化学方程式表示E中颜色变化的原因
(4)用F装置收集气体的依据是
考点:实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式,燃烧与燃烧的条件
专题:综合实验题
分析:(1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;白磷燃烧的条件是:与氧气接触,温度达到着火点;
(2)氧气不易溶于水,石灰石的主要成分是碳酸钙,稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳;
(3)显酸性的溶液能使石蕊试液变红色;
(4)根据氧气的密度比空气的大分析.
(2)氧气不易溶于水,石灰石的主要成分是碳酸钙,稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳;
(3)显酸性的溶液能使石蕊试液变红色;
(4)根据氧气的密度比空气的大分析.
解答:解:(1)过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,白磷与氧气接触时没有燃烧,说明温度没有达到白磷的着火点;
故填:2H2O2
2H2O+O2↑;温度没有达到白磷的着火点;
(2)C装置中,氧气不断增多,压强增大,把稀盐酸压入D中,能够观察到C中液面下降,稀盐酸与石灰石接触后,反应生成氯化钙、水和二氧化碳,能够观察到D中稀盐酸进入,有大量气泡产生,石灰石的主要成分是碳酸钙,碳酸钙和盐酸反应产生氯化钙、水和二氧化碳.
故填:C中液面下降;稀盐酸进入D中,产生大量气泡;CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)E中导管口有气泡冒出,说明二氧化碳进入石蕊试液中,二氧化碳能和石蕊试液中的水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色,因此溶液由紫色变为红色;
故填:CO2+H2O=H2CO3.
(4)因为氧气的密度比空气的大,所以利用向上排空气法收集;
故填:二氧化碳密度比空气大.
故填:2H2O2
| ||
(2)C装置中,氧气不断增多,压强增大,把稀盐酸压入D中,能够观察到C中液面下降,稀盐酸与石灰石接触后,反应生成氯化钙、水和二氧化碳,能够观察到D中稀盐酸进入,有大量气泡产生,石灰石的主要成分是碳酸钙,碳酸钙和盐酸反应产生氯化钙、水和二氧化碳.
故填:C中液面下降;稀盐酸进入D中,产生大量气泡;CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)E中导管口有气泡冒出,说明二氧化碳进入石蕊试液中,二氧化碳能和石蕊试液中的水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色,因此溶液由紫色变为红色;
故填:CO2+H2O=H2CO3.
(4)因为氧气的密度比空气的大,所以利用向上排空气法收集;
故填:二氧化碳密度比空气大.
点评:掌握氧气的反应原理、制取和收集方法;掌握二氧化碳的实验室制法及其物理性质和化学性质;注意燃烧与燃烧的条件.

练习册系列答案
相关题目
下列控制雾霾的措施正确的是( )
| A、直接燃烧煤炭 |
| B、露天焚烧秸秆 |
| C、大量使用燃油汽车 |
| D、充分利用太阳能 |
下列实验方案中设计不合理的是( )
| A、用燃烧的方法区分棉花、羊毛和合成纤维 |
| B、用石蕊溶液一次性鉴别盐酸、氢氧化钠溶液和蒸馏水三种物质 |
| C、测溶液pH时,将待测液滴到湿润的试纸上,再与标准比色卡比较 |
| D、电解水时加入少量的稀硫酸来增强水的导电性 |
下列化学方程式中有错误的是( )
| A、Fe+2HCl═FeCl2+H2↑ | ||||
| B、2NaOH+CuSO4═Cu(OH)2↓+Na2SO4 | ||||
| C、H2CO3═H2O+CO2↑ | ||||
D、S+O2
|