题目内容
19.如图1为元素周期表的一部分,请按要求填空:
(1)图1中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的核外电子层数 相同.
(2)根据图1中9号元素原子结构示意图可知在化学变化中易得到(填“得到”或“失去”)电子,该元素属于非金属(选填“金属”或“非金属”)元素,与图中17号氯元素化学性质相似.
(3)图2中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的原子层相同,最外层电子从左至右依次增加.
(4)根据图2信息可知钙元素的相对原子质量是40.08;氟元素的质子数为9.
分析 (1)根据元素周期表中同一周期的规定来分析;
(2)根据最外层电子数大于4的都易得电子,并且电子数越大越易得以及化合物的化学式写法进行分析;
(3)每一周期元素原子的原子层相同,最外层电子依次增加;
(4)根据表中信息分析解答.
解答 解:(1)第二周期的3-10号元素原子的电子层数相同,第三周期的11-18号元素原子的电子层数也相同,因此得出规律每一周期元素原子的电子层数相同;故答案为:核外电子层数;
(2)9号元素最外层电子数为7,都易得到电子而达到稳定结构,属于非金属;与17号氯元素的化学性质相似;答案:得到;非金属;17号氯元素;
(3)每一周期元素原子的原子层相同,最外层电子从左至右依次增加;答案:从左至右依次增加;
(4)根据图2信息可知钙元素的相对原子质量是40.08;氟元素的质子数为9.答案:40.08;9.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息、了解原子结构示意图的意义进行分析解题的能力.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
10.分子和原子的本质区别是( )
| A. | 分子能保持物质的化学性质而原子不能 | |
| B. | 分子间有间隙而原子间没有 | |
| C. | 化学变化中分子可以再分而原子不能再分 | |
| D. | 分子能构成物质而原子不能 |
4.下列现象中有一种变化和其他变化不同的是( )
| A. | 天然气燃烧 | B. | 石蜡熔化 | C. | 铝块压成铝箔 | D. | 西瓜榨汁 |
8. 现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.
现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.
(1)下列方法能检查该装置气密性的是AB.
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)MnO2催化下H2O2分解的符号表达式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O.
(3)甲小组有如下实验设计方案,完成下表.
(4)甲、乙两小组得出如图数据.
①甲组实验得出的数据可知:浓度越大,H2O2分解速率越快;
②由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下,H2O2在碱(填“酸”或“碱”)性环境下放出气体速率较快;乙组提出可以用Ba O2固体与硫酸(H2SO4)溶液反应制H2 O2,支持这一方案的理是过氧化氢在酸性环境下分解较慢.
 现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.
现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.(1)下列方法能检查该装置气密性的是AB.
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)MnO2催化下H2O2分解的符号表达式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O.
(3)甲小组有如下实验设计方案,完成下表.
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究浓度对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
①甲组实验得出的数据可知:浓度越大,H2O2分解速率越快;
②由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下,H2O2在碱(填“酸”或“碱”)性环境下放出气体速率较快;乙组提出可以用Ba O2固体与硫酸(H2SO4)溶液反应制H2 O2,支持这一方案的理是过氧化氢在酸性环境下分解较慢.
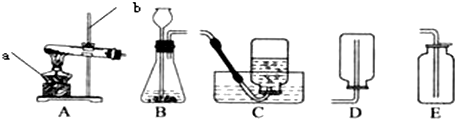
 小林同学设计如图所示的装置制取氧气
小林同学设计如图所示的装置制取氧气