题目内容
4.化合物M在空气中燃烧生成CO2和H2O,则下列物质中,不可能为M的是( )| A. | 甲烷 | B. | 葡萄糖 | C. | 一氧化碳 | D. | 酒精 |
分析 根据题意,化合物M在空气中燃烧生成CO2和H2O,由质量守恒定律,反应前后元素种类不变,可以确定该化合物的元素组成,进行分析判断.
解答 解:化合物M在空气中燃烧生成CO2和H2O,CO2和H2O两种物质中含有碳、氢、氧三种元素,根据质量守恒定律,反应前后,元素种类不变,反应物氧气中只含有氧元素,则某化合物中一定含有碳、氢两种元素,可能含有氧元素.
A、甲烷中含有碳元素和氢元素,符合要求,故选项错误.
B、葡萄糖中含有碳元素和氢元素,符合要求,故选项错误.
C、一氧化碳含有碳元素,不含氢元素,不符合要求,故选项正确.
D、酒精中含有碳元素和氢元素,符合要求,故选项错误.
故选:C.
点评 本题难度不大,掌握质量守恒定律(反应前后,元素种类不变)并能灵活运用是正确解答本题的关键.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
14.小婧同学学习了科学后知道,镁在氧气中燃烧会生成白色的氧化镁固体.但她在空气中点燃镁条时,却发现在生成的白色固体中还夹杂着少量的淡黄色固体.
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小婧查阅资料,记录了下列几种物质的颜色:
其他同学认为小婧不必查阅氯化镁的颜色,理由是空气的成分中不含氯元素;
【提出猜想】分析资料,小婧认为淡黄色固体可能是由镁与空气中的氮气(或N2)反应生成的;
【实验探究】小婧设计实验证实了自己的猜想,她的方案可能是将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体;
【实验结论】根据小婧的实验结果,写出镁条氮气中燃烧时的化学方程式:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
【反思与评价】通过上述实验,你对燃烧有什么新的认识?燃烧不一定要有氧气参加.
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小婧查阅资料,记录了下列几种物质的颜色:
| 物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
【提出猜想】分析资料,小婧认为淡黄色固体可能是由镁与空气中的氮气(或N2)反应生成的;
【实验探究】小婧设计实验证实了自己的猜想,她的方案可能是将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体;
【实验结论】根据小婧的实验结果,写出镁条氮气中燃烧时的化学方程式:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
【反思与评价】通过上述实验,你对燃烧有什么新的认识?燃烧不一定要有氧气参加.
13.如图所示,用玻璃杯罩住两支燃烧的蜡烛,一段时间后,下列现象与结论正确的是( )

| A. | 低的蜡烛先灭,因为二氧化碳的密度比空气的密度大 | |
| B. | 高的蜡烛先灭,气体受热膨胀,二氧化碳会上升,聚在玻璃杯的上方 | |
| C. | 该实验说明人从着火的房间逃离时,必须呈站立姿势跑出 | |
| D. | 两只蜡烛同时熄灭,因为玻璃杯中充满了二氧化碳气体 |
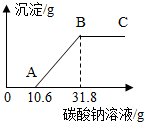 在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验:
在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验: 某补钙剂说明书的部分信息如图所示,现将20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应.反应后称得剩余物的质量为55.6g.
某补钙剂说明书的部分信息如图所示,现将20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应.反应后称得剩余物的质量为55.6g.

