题目内容
16.化学课后,某兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究.【提出问题1】该氢氧化钠溶液是否变质了呢?
【设计方案、进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡 | 产生气泡 | 氢氧化钠溶液一定变质了 |
【猜想与假设】猜想1:氢氧化钠溶液部分变质 猜想2:氢氧化钠溶液全部变质.
【查阅资料】氯化钙溶液呈中性,碳酸钠溶液呈碱性
【设计方案、进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡 | 有白色沉淀生成 | 说明原溶液中一定有碳酸钠,相关的反应方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液 | 溶液变红色 | 说明原溶液中一定含有氢氧化钠 |
【反思与评价】
(1)氢氧化钠溶液露置与空气中容易变质,请写出相关反应的化学方程式:2NaOH+CO2═Na2CO3+H2O.
(2)在上述【实验探究2】的实验中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案不可行(填“可行”或“不可行”).
分析 【设计方案、进行实验】
氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳;
【设计方案、进行实验】
碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
碳酸钠溶液和氢氧化钠溶液都是显碱性的溶液,都能使酚酞试液变红色;
【反思与评价】
碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠.
解答 解:【设计方案、进行实验】
取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡,产生气泡,说明溶液中含有碳酸钠,即氢氧化钠溶液已经变质,实验过程如下表所示:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡 | 产生气泡 | 氢氧化钠溶液一定变质了 |
(1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡,产生白色沉淀,说明原溶液中一定有碳酸钠,碳酸钠和氯化钙反应生成了碳酸钙沉淀和氯化钠,反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液,溶液变红色,说明原溶液中一定含有氢氧化钠,实验过程如下表所示:
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡 | 有白色沉淀生成 | 说明原溶液中一定有碳酸钠,反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液 | 溶液变红色 | 说明原溶液中一定含有氢氧化钠 |
(1)氢氧化钠溶液露置与空气中容易变质,是因为氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O.
故填:2NaOH+CO2═Na2CO3+H2O.
(2)不能用氢氧化钙溶液代替氯化钙溶液,这是因为碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,生成的氢氧化钠影响对原溶液中氢氧化钠的检验.
故填:不可行.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列各组物质中,前者不是后者溶质的是( )
| A. | 氯化钠、食盐水 | B. | 碘、碘酒 | C. | 氯化氢、盐酸 | D. | 氧化钙、石灰水 |
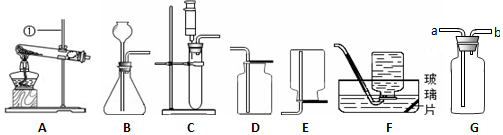
18. 某同学设计了如图所示的装置探究铁锈蚀的条件.a管中装入少量煮沸的蒸馏水,b管中是干燥的空气.调节L端与R端的液面高度一致,塞紧木塞.一段时间后观察.下列推断错误的是( )
某同学设计了如图所示的装置探究铁锈蚀的条件.a管中装入少量煮沸的蒸馏水,b管中是干燥的空气.调节L端与R端的液面高度一致,塞紧木塞.一段时间后观察.下列推断错误的是( )
 某同学设计了如图所示的装置探究铁锈蚀的条件.a管中装入少量煮沸的蒸馏水,b管中是干燥的空气.调节L端与R端的液面高度一致,塞紧木塞.一段时间后观察.下列推断错误的是( )
某同学设计了如图所示的装置探究铁锈蚀的条件.a管中装入少量煮沸的蒸馏水,b管中是干燥的空气.调节L端与R端的液面高度一致,塞紧木塞.一段时间后观察.下列推断错误的是( )| A. | 只有a管中的铁钉会锈蚀 | B. | L端与R端的液面高度仍然保持一致 | ||
| C. | 该实验说明铁的锈蚀和水有关 | D. | 该实验说明铁的锈蚀与空气有关 |

 ”、“
”、“ ”表示不同种元素的原子.
”表示不同种元素的原子.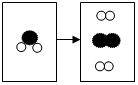
 B、
B、 C、
C、
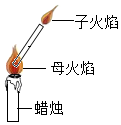 1860年,英国化学家法拉第在为少年儿童所做的化学讲座中用蜡烛和玻璃导管做了一个十分有趣的“子母火焰”实验,如图.
1860年,英国化学家法拉第在为少年儿童所做的化学讲座中用蜡烛和玻璃导管做了一个十分有趣的“子母火焰”实验,如图.