题目内容
12.称取氯化钠和氯化钙的固体混合物14g,放入烧杯中,加入96g碳酸钠溶液恰好完全反应.待反应完全后过滤,称得滤液的总质量为100g,试计算反应后所得溶液的溶质质量分数是多少?分析 根据质量守恒定律可知,过程中溶液的质量的减少是因为生成了沉淀碳酸钙,所以可以求算碳酸钙的质量,根据碳酸钙和对应的化学方程式求算生成的氯化钠和氯化钙的质量,进而求算原混合物中氯化钠的质量,最后求算溶液中溶质氯化钠的对应的质量分数.
解答 解:生成沉淀的质量为:14g+96g-100g=10g;
设:参加反应的CaCl2质量为x,生成的氯化钠质量为y
CaCl2+Na2CO3=CaCO3↓+2NaCl
111 100 117
x 10g y
$\frac{111}{x}=\frac{100}{10g}=\frac{117}{y}$
x=11.1g,y=11.7g
溶液中溶质NaCl的质量是14g-11.1g+11.7=14.6g
所得溶液的溶质质量分数为:$\frac{14.6g}{100g}×100%$=14.6%
答:所得溶液的溶质质量分数为14.6%.
点评 本题主要考查学生运用化学方程式进行计算的能力.学生须认真分析题意,找出各物质间的关系,正确写出方程式,并能根据质量分数公式计算,才能正确解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.下列实验操作正确的是( )
| A. |  稀释浓硫酸 | B. | 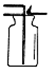 验证CO2集满 | C. | 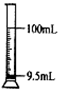 量取液体 | D. | 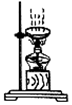 溶液蒸发 |
20.下列说法中错误的是( )
| A. | 铝比铁活泼,但比铁耐腐蚀 | |
| B. | 正常雨水的pH小于7 | |
| C. | 配制溶液时,搅拌可以增大固体的溶解度 | |
| D. | 有机化合物都含有碳元素,含有碳元素的化合物不一定是有机物 |
7.将锌粉和铁粉的混合物加入盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,将所得滤渣放入稀盐酸中,有气泡产生.下列说法错误的是( )
| A. | 滤液中最多含有两种溶质 | |
| B. | 滤液中一定含有Zn(NO3)2,可能含有Fe(NO3)2 | |
| C. | 滤渣里一定含有Fe和Ag,可能含有Zn | |
| D. | 若反应后所得滤液呈浅绿色,则滤渣中一定含有Fe和Ag,可能含有Zn |
17.以下是一个化学反应的微观示意图,从示意图获取的信息正确的是( )

| A. | 该反应的基本类型是化合反应 | |
| B. | 反应前后原子的种类与数目发生改变 | |
| C. | 反应前后两种分子的个数比是1:2 | |
| D. | 反应前后分子种类不发生改变 |
1.将无水硫酸亚铁(FeSO4)隔绝空气加强热,该反应的化学方程式为:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO3+X,则X的化学式( )
| A. | SO2 | B. | O2 | C. | H2O | D. | S |
2.下列有关物质用途的表述正确的是( )
| A. | 小苏打能与酸反应,可用于治疗胃酸过多 | |
| B. | 甲醛能使蛋白质变性,可用于食用水产品防腐 | |
| C. | 工业用盐有咸味,可用于腌制食品 | |
| D. | 活性炭具有吸附性,可用于自来水杀菌消毒 |