题目内容
13.有一种由CO、CO2、H2、水蒸气四种气体组成的混合气体,为了证明其中含有CO和H2,我们选用以下的仪器及药品设计实验:(已知浓硫酸可以吸收水蒸气)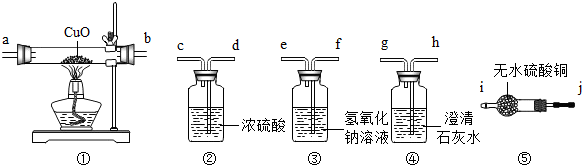
(1)在设计实验的过程中,我们准备当出现无水硫酸铜变成蓝色现象时证明有H2,水蒸气的存在对其有干扰;当出现澄清石灰水变浑浊现象时证明有CO,二氧化碳的存在对其有干扰.
(2)实验时,连接装置的顺序是③②①⑤④;导管接口的顺序是fedcabjihg.
分析 证明含有一氧化碳和氢气,需要先除去二氧化碳和水蒸气,除去二氧化碳的试剂用氢氧化钠溶液,除去水蒸气的试剂用浓硫酸,一氧化碳和氢气出的检验需要根据反应产物进行实验,所以先将混合气通过灼热的氧化铜生成二氧化碳和水蒸气,显通过无水硫酸铜检验水蒸气的生成,再通过澄清石灰水检验二氧化碳的存在.
解答 解:证明含有一氧化碳和氢气,需要先除去二氧化碳和水蒸气,除去二氧化碳的试剂用氢氧化钠溶液,除去水蒸气的试剂用浓硫酸,一氧化碳和氢气出的检验需要根据反应产物进行实验,所以先将混合气通过灼热的氧化铜生成二氧化碳和水蒸气,显通过无水硫酸铜检验水蒸气的生成,再通过澄清石灰水检验二氧化碳的存在.
(1)通过分析可知,在设计实验的过程中,当出现无水硫酸铜变成蓝色现象时证明有H2,水蒸气的存在对其有干扰;当出现澄清石灰水变浑浊现象时证明有CO,二氧化碳的存在对其有干扰;
(2)实验时,导气管是顺序是先用氢氧化钠溶液除去二氧化碳,用浓硫酸除去水蒸气,利用一氧化碳、氢气和氧化铜反应生成二氧化碳、水蒸气检验一氧化碳、氢气的存在,先利用干燥管内的无水硫酸铜检验水蒸气的存在,再利用澄清石灰水检验二氧化碳的存在,洗气装置的导气管时长进短出,所以实验时,连接装置的顺序是③②①⑤④,导管接口的顺序是fedcabjihg.
故答案为:(1)无水硫酸铜变成蓝色,水蒸气;澄清石灰水变浑浊,二氧化碳;
(2)③②①⑤④,fedcabjihg.
点评 本题考查了常见气体的检验和除杂,主要是混合气检验时需要出去杂质气体,再利用需要检验气体的性质设计实验过程,根据特征现象进行判断.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
3.工业制纯碱,是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,它的反应原理可用下列化学方程式表示:
NH3+CO2+H2O=NH4HCO3 …①
NH4HCO3+NaCl(饱和)=NaHCO3↓+NH4Cl …②
将所得碳酸氢钠晶体加热分解后即可得到纯碱.请回答:
(1)工业所制纯碱中常含有少量的氯化钠杂质,其原因是结晶析出的碳酸氢钠晶体表面沾有从溶液中带出的少量氯化钠.
(2)现有甲、乙两组的学生,欲测定某工业纯碱样品中Na2CO3的质量分数,分别设计并完成实验如下.
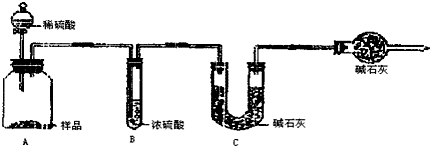
甲组:取10.00g样品,利用上图所示装置,测出反应后装置C中碱石灰的增重为3.3g.
乙组:取10.00g样品,向其中加入过量的盐酸,直至样品中无气泡冒出,加热蒸发所得物并在干燥器中冷却至室温后称量.反复加热、冷却、称量,直至所称量的固体质量几乎不变为止,此时所得固体的质量为10.99g.
请分析、计算后填表:
NH3+CO2+H2O=NH4HCO3 …①
NH4HCO3+NaCl(饱和)=NaHCO3↓+NH4Cl …②
将所得碳酸氢钠晶体加热分解后即可得到纯碱.请回答:
(1)工业所制纯碱中常含有少量的氯化钠杂质,其原因是结晶析出的碳酸氢钠晶体表面沾有从溶液中带出的少量氯化钠.
(2)现有甲、乙两组的学生,欲测定某工业纯碱样品中Na2CO3的质量分数,分别设计并完成实验如下.

甲组:取10.00g样品,利用上图所示装置,测出反应后装置C中碱石灰的增重为3.3g.
乙组:取10.00g样品,向其中加入过量的盐酸,直至样品中无气泡冒出,加热蒸发所得物并在干燥器中冷却至室温后称量.反复加热、冷却、称量,直至所称量的固体质量几乎不变为止,此时所得固体的质量为10.99g.
请分析、计算后填表:
| 分析与计算 | 计算样品中碳酸钠的质量分数 | 对实验结果的评价 | 实验失败的主要原因及对结果的影响 |
| 甲组 | 79.5% | 失败 | 加入的稀硫酸没有完全将碳酸钠反应掉,且没有冷却至室温,部分二氧化碳存在于装置内,没有被C装置内的碱石灰所吸收,造成测量结果偏小 |
| 乙组 | 99.6% | 成功 |
4.25℃时,向100g质量分数为5%的氯化钠溶液中加入5g氯化钠粉末,完全溶解后,溶液中氯化钠的质量分数为( )
| A. | 5% | B. | 9.5% | C. | 10% | D. | 无法计算 |
1.下列有关药品取用的说法正确的是( )
| A. | 实验中剩余的药品应该放回原瓶中 | |
| B. | 为避免中毒,不允许闻任何药品的气味 | |
| C. | 当未指明用量时,液体应取最少量即l-2ml | |
| D. | 当未指明用量时,固体应盖满容器底部即可 |
18.能准确描述水的物理性质的是( )
| A. | 水不能燃烧 | B. | 在标准状况下,水在4℃时密度最大 | ||
| C. | 水的沸点是100℃ | D. | 水电解可得到两种气体 |
5.下列关于结晶和晶体的说法,错误的是( )
| A. | 饱和溶液降温析出晶体后的溶液仍然是饱和溶液 | |
| B. | 降低饱和溶液的温度不一定有晶体析出 | |
| C. | 从溶液中析出的晶体不一定有结晶水 | |
| D. | 把溶液的溶剂蒸发一些一定会有晶体析出 |

 稀盐酸与100g溶质质量分数为20%的氢氧化钠溶液反应时,溶液的pH随加入溶液的质量m的变化关系如图所示.
稀盐酸与100g溶质质量分数为20%的氢氧化钠溶液反应时,溶液的pH随加入溶液的质量m的变化关系如图所示.