题目内容
6.过氧化钠(化学式为Na2O2)是一种淡黄色的固体物质,它能与水发生化学反应,其反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑,现将一定质量的过氧化钠加入到盛有175.2g氢氧化钠溶液的烧杯中,反应完毕后称得溶液的质量比反应前过氧化钠和水的总质量减少了6.4g,所得溶液中溶质的质量分数为20%,试计算:烧杯中的氢氧化钠溶液中溶质的质量分数.分析 根据质量守恒定律可以知道溶液反应前后减少的质量为氧气的质量;根据生成的氧气的质量结合反应的化学方程式可以计算出反应生成的氢氧化钠的质量,然后根据反应后所得溶液的质量分数计算出氢氧化钠的总质量,最后计算出原氢氧化钠溶液中氢氧化钠的质量,进而计算出氢氧化钠溶液的质量分数.
解答 解:根据质量守恒定律可以知道溶液反应前后减少的质量为氧气的质量,即为6.4g;
设参加反应的过氧化钠的质量为x,生成的氢氧化钠的质量为y.
2Na2O2+2H2O═4NaOH+O2↑
156 160 32
x y 6.4g
$\frac{156}{x}=\frac{160}{y}=\frac{32}{6.4g}$
解得:x=31.2g,y=32g
反应后溶液的质量为:31.2g+175.2g-6.4g=200g
所以反应后溶液中氢氧化钠的质量为:200g×20%=40g
烧杯中的氢氧化钠溶液中溶质的质量分数为$\frac{40g-32g}{175.2g}×$100%═4.6%
答:烧杯中的氢氧化钠溶液中溶质的质量分数为4.6%.
点评 要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景,结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地解答即可.

练习册系列答案
相关题目
16.下列有关化学用语中数字“2”的意义的说法,错误的是( )
①2SO2 ②Mg2+ ③CO2 ④$\stackrel{+2}{Cu}$SO4 ⑤O2- ⑥H2O2.
①2SO2 ②Mg2+ ③CO2 ④$\stackrel{+2}{Cu}$SO4 ⑤O2- ⑥H2O2.
| A. | 表示分子个数的是① | |
| B. | 表示离子所带电荷数的是②⑤ | |
| C. | 表示化合价数值的是④ | |
| D. | 表示一个分子中含有某种原子个数的是①③⑥ |
17.以下是某同学梳理的知识点
①造成酸雨的气体是二氧化硫和二氧化碳;
②可以用水来区分氢氧化钠固体和氯化钠固体
③稀有气体的原子最外层都是8个电子;
④用紫色石蕊溶液可以区分石灰水、稀盐酸和食盐水
⑤可以用灼烧方法来区分羊毛和化纤;
⑥为了增强肥效,将铵盐类氮肥和草木灰(碱性)混合施用
其中正确的是( )
①造成酸雨的气体是二氧化硫和二氧化碳;
②可以用水来区分氢氧化钠固体和氯化钠固体
③稀有气体的原子最外层都是8个电子;
④用紫色石蕊溶液可以区分石灰水、稀盐酸和食盐水
⑤可以用灼烧方法来区分羊毛和化纤;
⑥为了增强肥效,将铵盐类氮肥和草木灰(碱性)混合施用
其中正确的是( )
| A. | ②④⑤ | B. | ①②⑤ | C. | ③⑤⑥ | D. | ②③④⑤ |
14.下列关于催化剂的说法正确的是( )
| A. | 化学反应前后,催化剂的质量和化学性质都不变 | |
| B. | 催化剂可以提高化学反应的速率 | |
| C. | 催化剂可以增加生成物的质量 | |
| D. | 任何化学反应都需要催化剂 |
1.下列实验操作中,正确的是( )
| A. |  倾倒液体 | B. | 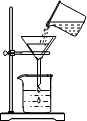 过滤 | C. | 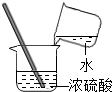 稀释浓硫酸 | D. | 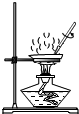 蒸发 |
18.2015年2月28日,前央视记者柴静的《雾霾深度调查:穹顶之下》引发网友热议.形成雾霾天气的主要污染物是直径小于或等于2.5微米的悬浮颗粒物,即PM2.5.下列事实与形成PM2.5无关的是( )
| A. | 风力发电 | B. | 工业粉尘 | C. | 汽车尾气 | D. | 煤炭燃烧 |
15.下列四种氮肥各10kg,其中所含氮元素的质量最小的是( )
| A. | NH4HCO3 | B. | NH4NO3 | C. | (NH4)2SO4 | D. | CO(NH2)2 |
 2014年6月10日是“全国低碳日”,“节能减排,低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化碳的排放.下列做法符合“主题是C
2014年6月10日是“全国低碳日”,“节能减排,低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化碳的排放.下列做法符合“主题是C