题目内容
11.学校研究学习小组想测定Cu-Zn合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀盐酸和必要的仪器.研究小组取该合金的粉末32.5g,与足量该盐酸充分反应,经测定,产生了0.4g气体,试通过计算求出该合金中铜的质量分数.分析 根据氢气的质量求出锌的质量,再用合金质量减去锌的质量即为铜的质量.
解答 解:设合金中锌的质量是x,稀盐酸中溶质的质量为y.
Zn+2HCl=ZnCl2+H2↑
65 2
x 0.4g
$\frac{65}{x}=\frac{2}{0.4g}$,
x=13g
所以合金中铜的质量分数为$\frac{32.5g-13g}{32.5g}$×100%=60%
答:该合金中铜的质量分数是60%.
点评 本题考查了金属的性质以及根据化学方程式进行的计算,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
1.实验操作有误或不规范,很可能造成实验失败甚至酿成事故,下列实验操作正确的是( )
| A. | 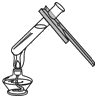 给液体加热 | B. | 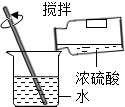 稀释浓硫酸 | ||
| C. | 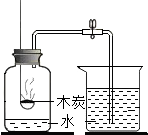 测定空气里氧气含量 | D. |  称量氢氧化钠 |
2.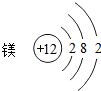 依据如图的原子结构示意图,下列说法正确的是( )
依据如图的原子结构示意图,下列说法正确的是( )
 依据如图的原子结构示意图,下列说法正确的是( )
依据如图的原子结构示意图,下列说法正确的是( )| A. | 该原子的核电荷数为12 | B. | 该原子核外有两个电子 | ||
| C. | 该原子在反应中易得到电子 | D. | 该原子在反应中容易成为阴离子 |
19.工业上通过以下反应将二氧化硅(SiO2)转化为硅:SiO2+2C $\frac{\underline{\;高温\;}}{\;}$ Si+2CO↑,该反应属于( )
| A. | 置换反应 | B. | 分解反应 | C. | 复分解反应 | D. | 化合反应 |
3.(NH4)2CO3中氮元素的化合价为( )
| A. | -3 | B. | 0 | C. | +3 | D. | +5 |
1.张华同学对酸、碱、盐的知识进行了以下的梳理.
(1)填写下表空格中的化学式.
思考:根据以上盐中的金属元素的排列,可以得出他是依据金属活动性顺序归纳整理的.
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图.请你在右边的圆圈中填入适当的化学式或离子符号:

(3)张华同学发现酸、碱、盐之间的反应都有盐类物质生成.请写出一个能生成MgCl2的复分解反应的化学方程式:2HCl+Mg(OH)2=MgCl2+2H2O.
(4)我们知道溶液酸碱度pH可显示的溶液的酸碱性;酸溶液pH<7,溶液显酸性;碱溶液pH>7,溶液显碱性.提出问题:盐溶液的pH怎样呢?盐溶液显什么性呢?
猜想与假设:盐溶液的pH可能为:pH=7、pH<7、pH>7.
设计与实验:下列是两同学分别对相同的NaCl溶液、CuSO4溶液、K2CO3溶液的pH进行的测定实验:甲同学:取pH试纸放在玻片上,用玻棒蘸取测试液滴在pH试纸上,试纸显色后与pH标准比色卡比较.乙同学:取pH试纸放在玻片上,用蒸馏水将pH试纸润湿,再用玻棒蘸取测试液滴在pH试纸上,试纸显色后与pH标准比色卡比较.
记录数据:下表是两同学记录所测pH的实验数据:
结论:通过测定几种盐溶液的pH,可以得出的结论是:盐的溶液不一定呈中性.
评价与反思:上述两同学测得的数据,反映了溶液真实pH的是甲同学.
(1)填写下表空格中的化学式.
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | AlCl3 | ZnCl2 | FeCl2 | CuCl2 |
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图.请你在右边的圆圈中填入适当的化学式或离子符号:

(3)张华同学发现酸、碱、盐之间的反应都有盐类物质生成.请写出一个能生成MgCl2的复分解反应的化学方程式:2HCl+Mg(OH)2=MgCl2+2H2O.
(4)我们知道溶液酸碱度pH可显示的溶液的酸碱性;酸溶液pH<7,溶液显酸性;碱溶液pH>7,溶液显碱性.提出问题:盐溶液的pH怎样呢?盐溶液显什么性呢?
猜想与假设:盐溶液的pH可能为:pH=7、pH<7、pH>7.
设计与实验:下列是两同学分别对相同的NaCl溶液、CuSO4溶液、K2CO3溶液的pH进行的测定实验:甲同学:取pH试纸放在玻片上,用玻棒蘸取测试液滴在pH试纸上,试纸显色后与pH标准比色卡比较.乙同学:取pH试纸放在玻片上,用蒸馏水将pH试纸润湿,再用玻棒蘸取测试液滴在pH试纸上,试纸显色后与pH标准比色卡比较.
记录数据:下表是两同学记录所测pH的实验数据:
| NaCl溶液 | CuSO4溶液 | K2CO3溶液 | |
| 甲同学 | 7 | 4 | 10 |
| 乙同学 | 7 | 5 | 9 |
评价与反思:上述两同学测得的数据,反映了溶液真实pH的是甲同学.