题目内容
13.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如下图.下列说法正确的是( )
| A. | 该反应为分解反应 | B. | 参加反应的甲、丁质量比为1:2 | ||
| C. | 丙一定是该反应的催化剂 | D. | 丁相对分子质量是甲的2倍 |
分析 根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.反应后质量增加的是生成物,减少的是反应物,据此分析.
解答 解:根据质量守恒定律,反应前丙的质量为:4g+10g+3g+4g-(6g+4g+8g)=3g,甲、丁反应后质量减少,为反应物,乙反应后质量增加,为生成物.
A、甲、丁是反应物,乙是生成物,该反应为化合反应,故错误;
B、参加反应的甲、丁质量比为:(6g-4g):(8g-4g)=1:2,故说法正确;
C、丙反应前后质量不变,可能为催化剂,也可能不参加反应,故说法错误;
D、生成甲、丁的质量比为:(6g-4g):(8g-4g)=1:2,由于未知反应的化学方程式中的化学计量数,故无法确定甲、丁的相对分子质量关系,故说法错误;
故选B.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
相关题目
3.下列净化水的方法,净化程度最高的是( )
| A. | 沉降 | B. | 过滤 | C. | 蒸馏 | D. | 吸附 |
4.豆浆被称为“植物奶”,其中含有的异黄酮(C15H10O2)具有防癌功能,下列关于异黄酮说法正确的是( )
| A. | 异黄酮中共含有27个原子 | |
| B. | 一个异黄酮分子中含有一个氧分子 | |
| C. | 异黄酮中碳元素的质量分数最大 | |
| D. | 异黄酮中碳、氢、氧三种元素的质量比为15:10:2 |
1.某气体混合物由H2、N2、CO和CH4中的两种组成,将该混合气体点燃后的产物依次通过浓H2SO4和NaOH溶液,结果两溶液的质量均有增加.则该混合气体的组成不可能是( )
| A. | N2和CO | B. | H2和CO | C. | N2和CH4 | D. | H2和CH4 |
8.下列实验方案能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 证明某气体是二氧化碳 | 将燃着的小木条放入集气瓶中,木条熄灭 |
| B | 证明氢氧化钠溶液已变质 | 向溶液中滴加无色酚酞,溶液呈红色 |
| C | 除去NaOH溶液中的Ca(OH)2 | 向溶液中通入足量的CO2,过滤 |
| D | 鉴别CO和CH4 | 分别点燃,在火焰上方罩一干冷的烧杯 |
| A. | A | B. | B | C. | C | D. | D |
3.下列叙述完全正确的是( )
| A. | 碳酸钠溶液能使无色酚酞试液变红 | |
| B. | 过氧化氢是由氢原子和氧原子构成的,它与水的组成元素相同 | |
| C. | 某白色固体与熟石灰混合后加热,产生可使湿润的红色石蕊试纸变蓝的气体,证明该固体是铵盐 | |
| D. | 分子都是由不同原子构成的 |
10.如图a、b、c三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )


| A. | 将t2℃对a、c两种物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数相等 | |
| B. | C中混有少量a,可用降温结晶的方法提纯c | |
| C. | 将t2℃时a、b、c三种物质的饱和溶液降温至t1℃,祈出晶体最多的是a物质 | |
| D. | t2℃时,a溶液的溶质质量分数不一定大于b溶液的溶质质量分数 |
8.请你根据如图所示的溶解度曲线判断,下列说法中正确的是( )
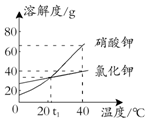

| A. | 氯化钾在20℃时的溶解度比硝酸钾大 | |
| B. | 将40℃的硝酸钾溶液降温至20℃,溶液中一定会有晶体析出 | |
| C. | 将等量的氯化钾和硝酸钾分别放于等量的水中,把温度调为t1℃,此时,二者的溶质质量分数相等 | |
| D. | 当温度高于t1℃时,饱和硝酸钾的溶剂质量分数比饱和氯化钾的大 |
