题目内容
20. 化学是以实验为基础的自然科学,通过实验现象的观察和分析得到结论.
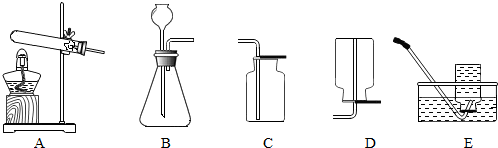
化学是以实验为基础的自然科学,通过实验现象的观察和分析得到结论.(1)A实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小,通过烧杯中的水倒吸入瓶内的体积来推测空气里氧气的含量.
(2)判断B实验中发生化学变化的依据是有黑色固体生成;有关的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
分析 通过测定空气里氧气含量的实验、铁丝在氧气张燃烧实验的原理可以得出本题的答案.
解答 解:(1)测定空气里氧气含量的实验原理是:红磷燃烧,消耗集气瓶中的氧气,从而使集气瓶内外产生压强差,烧杯中的水在压强差的作用下流入集气瓶中,继而测定出流入集气瓶中水的体积,再用水的体积与集气瓶的容积相比,就能得到实验的结论.故填:氧气;
(2)铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,生成物是四氧化三铁;故填:有黑色固体生成;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
点评 本题主要考查测定空气里氧气含量的实验、铁丝在氧气中燃烧实验的原理,难度稍大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.前年流行的猪流感,感染早期用药物“达菲”治疗有效.判断达菲的治疗机理中是否发生了化学变化,其依据是( )
| A. | 病毒的大小是否改变 | B. | 病毒的形状是否变化 | ||
| C. | 病毒是否离开宿主细胞 | D. | 是否有新物质生成 |
10. 向盛有固体的广口瓶中滴加分液漏斗中的液体,可观察到U形管中的红墨水液面左降右升,该固体和液体试剂不可能是( )
向盛有固体的广口瓶中滴加分液漏斗中的液体,可观察到U形管中的红墨水液面左降右升,该固体和液体试剂不可能是( )
 向盛有固体的广口瓶中滴加分液漏斗中的液体,可观察到U形管中的红墨水液面左降右升,该固体和液体试剂不可能是( )
向盛有固体的广口瓶中滴加分液漏斗中的液体,可观察到U形管中的红墨水液面左降右升,该固体和液体试剂不可能是( )| A. | 大理石和稀硫酸 | B. | 生石灰和水 | ||
| C. | 硝酸钾和水 | D. | 双氧水和二氧化锰 |


 探究燃烧条件的实验装置如图所示
探究燃烧条件的实验装置如图所示

 有一研究性学习小组为测定某铜锌合金的成分,取l0g该合金经粉碎后放入烧杯中,再加入93.7g质量分数为20%的稀硫酸(反应后硫酸有剩余),反应过程中烧杯内固体物质的质量与反应时间的关系如图所示.请回答下列问题:
有一研究性学习小组为测定某铜锌合金的成分,取l0g该合金经粉碎后放入烧杯中,再加入93.7g质量分数为20%的稀硫酸(反应后硫酸有剩余),反应过程中烧杯内固体物质的质量与反应时间的关系如图所示.请回答下列问题: