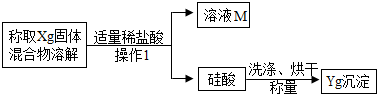
题目内容
将足量硝酸银溶液中滴加一定质量的稀盐酸,充分反应后测得所得溶液与原硝酸银溶液质量相等,则该稀盐酸中溶质的质量分数为________ (保留一位小数).
25.4%
分析:根据质量守恒定律“充分反应后测得所得溶液与原硝酸银溶液质量相等”说明硝酸银与盐酸反应后生成的沉淀氯化银的质量与加入的稀盐酸溶液的质量相等;由此根据化学方程式可求出稀盐酸中溶质的质量分数;
解答:设盐酸溶液中溶质氯化氢的质量为a;生成的沉淀氯化银的质量为b
AgNO3+HCl═AgCl↓+HNO3
36.5 143.5
a b
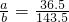
根据分析可知生成的沉淀氯化银的质量与加入的稀盐酸溶液的质量相等;
则该稀盐酸中溶质的质量分数为: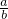 ×100%
×100%
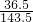 ×100%=25.4%
×100%=25.4%
故答案为;25.4%
点评:本题难度不是很大,主要考查了根据化学方程式计算有关物质的质量的计算,培养学生的分析问题、解决问题的能力.
分析:根据质量守恒定律“充分反应后测得所得溶液与原硝酸银溶液质量相等”说明硝酸银与盐酸反应后生成的沉淀氯化银的质量与加入的稀盐酸溶液的质量相等;由此根据化学方程式可求出稀盐酸中溶质的质量分数;
解答:设盐酸溶液中溶质氯化氢的质量为a;生成的沉淀氯化银的质量为b
AgNO3+HCl═AgCl↓+HNO3
36.5 143.5
a b
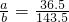
根据分析可知生成的沉淀氯化银的质量与加入的稀盐酸溶液的质量相等;
则该稀盐酸中溶质的质量分数为:
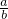 ×100%
×100%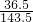 ×100%=25.4%
×100%=25.4%故答案为;25.4%
点评:本题难度不是很大,主要考查了根据化学方程式计算有关物质的质量的计算,培养学生的分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目