题目内容
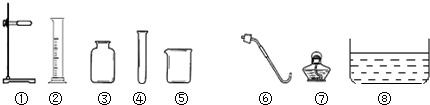
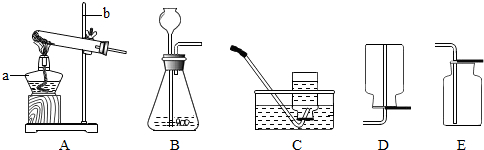
过氧化氢(H2O2)的水溶液俗称双氧水.实验室用以下两种方法制取氧气.请回答下列问题.
方法一:2KClO3
2KCl+3O2↑ 方法二:2H2O2
2H2O+O2↑
(1)方法一和方法二中MnO2都作为反应的
(2)现有500g双氧水,H2O2的质量分数为3.4%.则该溶液中H2O2的质量为
(3)用方法二,取上述质量的H2O2进行实验,最多可以制得氧气多少克?
方法一:2KClO3
| ||
| △ |
| ||
(1)方法一和方法二中MnO2都作为反应的
催化剂
催化剂
.比较两种方法,方法二的主要优点是不需加热,操作简单
不需加热,操作简单
.(2)现有500g双氧水,H2O2的质量分数为3.4%.则该溶液中H2O2的质量为
17
17
克.(3)用方法二,取上述质量的H2O2进行实验,最多可以制得氧气多少克?
分析:(1)二氧化锰在氯酸钾和过氧化氢分解反应中作催化剂,并根据过氧化氢溶液制取氧气与用氯酸钾制取氧气的具体操作进行分析比较;
(2)根据溶质的质量=溶液的质量×溶质的质量分数进行计算;
(3)根据过氧化氢的质量及过氧化氢溶液反应方程式进行计算.
(2)根据溶质的质量=溶液的质量×溶质的质量分数进行计算;
(3)根据过氧化氢的质量及过氧化氢溶液反应方程式进行计算.
解答:解:(1)二氧化锰在氯酸钾和过氧化氢分解反应中均作为反应的催化剂,过氧化氢溶液和二氧化锰制取氧气不需要加热,操作简单,节省能源,这是它的优点;
故答案为:催化剂;不需加热,操作简单;
(2)溶质的质量=溶液的质量×溶质的质量分数,所以过氧化氢的质量是:500g×3.4%=17g;
故答案为:17;
(3)设最多可以制取氧气的质量的质量是X
2H2O2
2H2O+O2↑
68 32
17g X
=
X=8g
答:最多可以制得氧气8克.
故答案为:催化剂;不需加热,操作简单;
(2)溶质的质量=溶液的质量×溶质的质量分数,所以过氧化氢的质量是:500g×3.4%=17g;
故答案为:17;
(3)设最多可以制取氧气的质量的质量是X
2H2O2
| ||
68 32
17g X
| 68 |
| 17g |
| 32 |
| X |
X=8g
答:最多可以制得氧气8克.
点评:本题既考查了根据化学方程式的计算,又考查了溶质的质量分数应用及对二氧化锰的了解、实验方案的评价等知识,注重基础,难度不大.

练习册系列答案
相关题目
 实验室中常用高锰酸钾受热分解制取氧气.
实验室中常用高锰酸钾受热分解制取氧气.