题目内容
7.某工厂化验室用稀盐酸测定造纸厂废水中氢氧化钠的质量分数,取废水样品100g倒入烧杯中,逐滴加入9.8%的稀硫酸至恰好完全反应,共用去稀硫酸50g,请计算:(温馨提示:H2SO4+2NaOH=Na2SO4+2H2O)
(1)中和废水所用硫酸的质量
(2)废水中氢氧化钠的质量分数.
分析 (1)根据溶质的质量分数的计算公式计算.
(2)利用恰好完全反应所消耗硫酸的质量和反应的化学方程式,计算废水中氢氧化钠的质量,最后利用溶液中溶质的质量分数公式计算出废水中氢氧化钠的质量分数.
解答 解:(1)反应消耗硫酸的质量为:50 g×9.8%=4.9 g
(2)设废水样品中氢氧化钠的质量为x.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
x 4.9 g
$\frac{80}{98}=\frac{x}{4.9g}$ 解得:x=4g
废水中氢氧化钠的质量分数为:$\frac{4g}{100g}×100%$=4%.
答:(1)中和废水所用硫酸的质量是4.9g;(2)废水中氢氧化钠的质量分数是4%.
点评 本题属于有关溶质质量分数和化学方程式的基本计算,难度不大,注意计算的数据要准确.

练习册系列答案
相关题目
15.一些食物pH 的近似值范围如下:橘子汁3.~4.0;泡菜3.2~3.6;牛奶6.3~6.6;鸡蛋清7.6~8.0.下列说法中,不正确的是( )
| A. | 鸡蛋清显碱性 | B. | 胃酸过多的人应少吃泡菜 | ||
| C. | 橘子汁能使紫色石蕊溶液变红 | D. | 牛奶比橘子汁的酸性强 |
3.下列四个图象中,能正确反映对应变化关系的是( )
| A. | 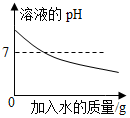 在常温下,稀释KOH溶液,加入水的质量与溶液pH变化的关系 | |
| B. | 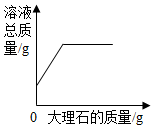 向一定量的稀盐酸中加入大理石,溶液的总质量随加入的大理石的质量关系 | |
| C. | 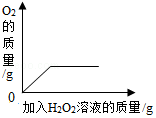 向盛有少量二氧化锰的烧杯中不断地加入过氧化氢溶液,产生的氧气与加入的过氧化氢溶液的情况 | |
| D. | 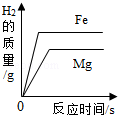 将等质量的镁片和铁片投入到足量稀硫酸中,产生氢气的质量随时间变化关系 |
10.如图是某反应的微观示意图,以下说法正确的是( )

| A. | 分子是化学变化中最小粒子 | |
| B. | 如图表示的微观变化过程中共有三种分子 | |
| C. | 该反应有单质生成 | |
| D. | 参加反应的“ ”分子与“ ”分子与“ ”分子的个数比为1:3 ”分子的个数比为1:3 |
7.X、Y、Z三种元素的化合价分别为+1,+7,-2,则这三种元素所组成的化合物的化学式可能为( )
| A. | XYZ | B. | X2YZ4 | C. | XYZ4 | D. | X2YZ3 |
8.某环保监测站取刚降下的雨水,某隔一段时间测定其pH,数据如表.下列有关说法不正确的是( )
| 时间/min | 0 | 1 | 2 | 4 | 5 |
| pH | 4.8 | 4.6 | 4.5 | 4.5 | 4.5 |
| A. | 雨水酸性逐渐减弱 | |
| B. | 雨水的酸性一段时间后趋于稳定 | |
| C. | 酸雨会腐蚀机械设备 | |
| D. | 硫和氮的氧化物是形成酸雨的主要因素 |
 a、b、c三种固体物质的溶解度曲线如图所示,请回答:
a、b、c三种固体物质的溶解度曲线如图所示,请回答: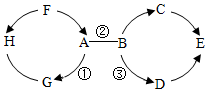 A~H为初中化学常见物质.其中A、E为氧化物且E为常见的液体,B、D为碱,H、G为单质,C为石灰石的主要成分,F为胃酸的主要成分;反应①为光合作用.它们之间的相互关系如图所示.其中“→”表示转化关系,“-”表示相互之间能发生反应(部分反应物、生成物以及反应条件省略).
A~H为初中化学常见物质.其中A、E为氧化物且E为常见的液体,B、D为碱,H、G为单质,C为石灰石的主要成分,F为胃酸的主要成分;反应①为光合作用.它们之间的相互关系如图所示.其中“→”表示转化关系,“-”表示相互之间能发生反应(部分反应物、生成物以及反应条件省略).