题目内容
20.华裔科学家高锟因提出“以高纯度的石英玻璃制造光纤”,获得2009年诺贝尔奖.工业上以石英砂(主要成分SiO2)制取高纯度石英玻璃的生产原理如下:
请回答下列问题:
(1)已知反应①的另一产物是有毒气体,其化学式为CO.
(2)已知反应②为化合反应,该反应的化学方程式为Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4.
(3)已知反应③除生成二氧化硅外还有一种气体生成,则反应③的化学方程式为SiCl4+O2 $\frac{\underline{\;1300℃\;}}{\;}$SiO2+2Cl2.
(4)将反应③中的氧气换成氢气,可制得生产计算机芯片的高纯硅,则另一产物的化学式为HCl.
分析 (1)根据二氧化硅和碳反应生成有毒气体,根据反应中元素种类不变可确定该产物进行解答;
(2)根据化合反应是两种或两种以上物质反应生成一种物质的化学变化进行解答;
(3)根据置换反应是一种单质与一种化合生成一种单质与一种化合的反应进行解答;
(4)根据化学反应前后元素的种类不变即可求出另一产物的化学式.
解答 解:(1)二氧化硅和碳反应生成有毒气体,根据反应中元素种类不变,可确定该产物为一氧化碳;故答案为:CO;
(2)反应②为两种物质生成一种物质的化合反应,所以是硅和氯气反应生成四氯化硅,反应的化学方程式为Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4;故答案为:Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4;
(3)反应③为单质与化合物生成单质与化合物的置换反应,根据反应中元素种类不变,可确定另一单质生成物为氯气,所以反应的化学方程式为SiCl4+O2$\frac{\underline{\;1300℃\;}}{\;}$SiO2+2Cl2;故答案为:SiCl4+O2 $\frac{\underline{\;1300℃\;}}{\;}$SiO2+2Cl2;
(4)反应物为氢气和四氯化硅生成物有硅,根据反应中元素种类不变,可确定另一元素中含有氢、氯元素,所以则另一产物的化学式为HCl;故答案为:HCl.
点评 对知识进行迁移解决情形相似的新问题是本题的特点,体现出知识运用与问题分析的能力.

练习册系列答案
相关题目
10.下列说法中正确的是( )
| A. | 原子的质量几乎都集中在原子核中 | |
| B. | 生活中常接触到的“高钙牛奶”、“碘盐”中的“钙”、“碘”指的是离子 | |
| C. | 用灯帽盖灭酒精灯,是为了降低可燃物的温度 | |
| D. | 淡水资源丰富,所以淡水资源可以取之不尽,用之不竭 |
11.下列图象能正确反映其对应操作中各量变化关系的是( )
| A. | 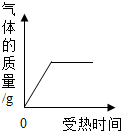 用一定质量的高锰酸钾加热制氧气 用一定质量的高锰酸钾加热制氧气 | |
| B. | 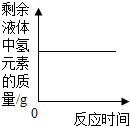 过氧化氢溶液与二氧化锰混合物制取氧气 过氧化氢溶液与二氧化锰混合物制取氧气 | |
| C. | 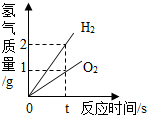 电解水实验 电解水实验 | |
| D. | 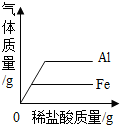 分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量 分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量 |
5.分析推理是化学常用的一种学习方法,下列推理正确的是( )
| A. | MnO2可以加快H2O2分解产生O2的速率,所以催化剂一定加快化学反应速率 | |
| B. | 钙原子核钙离子的质子数都是2O,所以质子数相同的微粒一定是同种元素 | |
| C. | 化学变化中分子一定发生改变,所以分子发生改变的变化一定是化学变化 | |
| D. | Na+、Mg2+、Cl-的最外层电子数均为8,由此得出离子的最外层电子数均为8 |
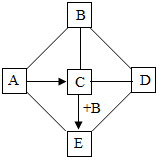 已知A-E是初中化学的常见物质.A和D是两种常见的碱;B是一种常见的酸,且只含
已知A-E是初中化学的常见物质.A和D是两种常见的碱;B是一种常见的酸,且只含