题目内容
元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息.
请认真分析表中信息,回答下列问题:
(1)地壳中含量仅次于氧的非金属元素名称是 ,该元素原子核内的质子数为 .
(2)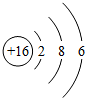 所表示的粒子符号为 .
所表示的粒子符号为 .
(3)由原子序数为11和17的两种元素组成的化合物是 .
(4)在元素周期表中存在很多规律,例如: .
| 1 H 氢 | 2 He 氦 | |||||||
| 3 Li 锂 | 4 Be 铍 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 | |
| 11 Na 钠 | 12 Mg 镁 | 13 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氩 | |
(1)地壳中含量仅次于氧的非金属元素名称是
(2)
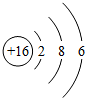 所表示的粒子符号为
所表示的粒子符号为(3)由原子序数为11和17的两种元素组成的化合物是
(4)在元素周期表中存在很多规律,例如:
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据地壳中各元素含量解答;
(2)根据原子结构示意图的判断方法来分析;
(3)根据两种元素的化合价可以写出其组成化合物的化学式;
(4)根据对元素周期表的观察和元素周期律进行分析解答本题.
(2)根据原子结构示意图的判断方法来分析;
(3)根据两种元素的化合价可以写出其组成化合物的化学式;
(4)根据对元素周期表的观察和元素周期律进行分析解答本题.
解答:解:(1)地壳中元素含量由高到低的顺序是氧、硅、铝、铁,仅次于氧的非金属元素名称是硅,硅原子的质子数为14;故填:硅;14;
(2)该粒子核内质子数为16,属于硫元素,核内质子数=核外电子数,属于原子,该符号是硫原子,故填:S;
(3)原子序数为11元素为钠元素,原子序数为17的元素为氯元素,钠为+1价,氯为-1价,故组成化合物的化学式为NaCl.故填:NaCl;
(4)根据对元素周期表的观察可总结:元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束(第一周期从非金属元素氢开始);故答案为:每周期都是以稀有气体元素结束(或由金属元素逐渐过渡到非金属元素).
(2)该粒子核内质子数为16,属于硫元素,核内质子数=核外电子数,属于原子,该符号是硫原子,故填:S;
(3)原子序数为11元素为钠元素,原子序数为17的元素为氯元素,钠为+1价,氯为-1价,故组成化合物的化学式为NaCl.故填:NaCl;
(4)根据对元素周期表的观察可总结:元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束(第一周期从非金属元素氢开始);故答案为:每周期都是以稀有气体元素结束(或由金属元素逐渐过渡到非金属元素).
点评:本题考查学生对元素周期表中的一些变化规律的归纳和总结以及对元素周期表的应用.

练习册系列答案
相关题目
符号N5+是( )
| A、混合物 | B、单质 |
| C、一个分子 | D、一个离子 |
某化工厂以石灰石、纯碱和水为主要原料制取烧碱.在制取过程中的变化关系为CaCO3→CaO→Ca(OH)2→NaOH;上述变化过程中没有涉及的化学反应基本类型是( )
| A、化合反应 | B、分解反应 |
| C、置换反应 | D、复分解反应 |
通过实验分析,测得某种氯化物中氯元素的质量分数为47.65%,这种物质可能( )
| A、NaCl |
| B、KCl |
| C、CaCl2 |
| D、MgCl2 |
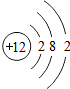 ,镁原子在化学反应中容易
,镁原子在化学反应中容易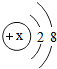 ,若表示原子,则x
,若表示原子,则x