题目内容
5.下列说法不正确的是( )| A. | 直接品尝实验室药品的味道 | |
| B. | “侯氏制碱法”生产的“碱”是指碳酸钠 | |
| C. | 误食重金属盐,可服牛奶或鸡蛋清解毒 | |
| D. | 液化气起火,迅速关闭阀门,以断绝可燃物的来源 |
分析 A、根据实验室药品不能品尝进行解答;
B、侯氏制碱法制得的“碱”是纯碱,即碳酸钠;
C、根据重金属盐能使蛋白质失去生理活性,而使人中毒进行解答;
D、根据关闭阀门是隔绝氧气进行解答.
解答 解:A、实验室药品不能品尝,故A错误;
B、侯氏制碱法制得的“碱”是纯碱,即碳酸钠,故B正确;
C、重金属盐能使蛋白质失去生理活性,而使人中毒,所以误食重金属盐,可服牛奶或鸡蛋清解毒,故C正确;
D、液化气起火,迅速关闭阀门,断绝可燃物的来源,故D正确.
故选:A.
点评 本题考查学生药品的使用、“侯氏制碱法”的原理以及重金属盐中毒的原因的知识,可以根据所学知识来回答,难度不大.

练习册系列答案
相关题目
11.下列是关于溶液的一些图表和图象,请根据图示回答问题:

(1)甲、乙两种固体物质的溶解度曲线如图1所示,分析并回答下列问题.
①图1中,溶解度随温度升高而减小的是乙.
②20℃时,将等质量的甲、乙分别加入盛有等质量水的试管中,充分溶解后如图2所示.据此推断,图1中温度t>(填“>”“<”或“=”)20℃.
(2)某烧杯中盛有一定质量、温度为60℃的甲溶液,将其置于室温环境中,测定不同温度时析出固体甲的质量.测定结果记录如下表.
若不考虑水蒸发对实验的影响,请思考:50℃时,该溶液是否为饱和溶液?无法判断(填“是”“否”或“无法判断”).

(1)甲、乙两种固体物质的溶解度曲线如图1所示,分析并回答下列问题.
①图1中,溶解度随温度升高而减小的是乙.
②20℃时,将等质量的甲、乙分别加入盛有等质量水的试管中,充分溶解后如图2所示.据此推断,图1中温度t>(填“>”“<”或“=”)20℃.
(2)某烧杯中盛有一定质量、温度为60℃的甲溶液,将其置于室温环境中,测定不同温度时析出固体甲的质量.测定结果记录如下表.
| 溶液的温度/℃ | 55 | 50 | 40 | 30 | 20 |
| 析出固体甲的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
20.如图为三种常见元素的周期表中的信息,以下说法中正确的是( )


| A. | 硅元素在地壳中含量最多 | B. | 氮元素核外有7个质子 | ||
| C. | 氮元素和氧元素只能组成一种物质 | D. | 硅元素的相对原子质量为28.09 |
10.下列各组物质在给定pH的溶液中能大量共存并形成无色溶液的是( )
| A. | pH为12:BaCl2、Na2CO3、NaOH | B. | pH为1:NaOH、KHCO3、Na2SO4 | ||
| C. | pH为2:KNO3、NaCl、H2SO4 | D. | pH为3:FeCl3、CuSO4、KCl |
17.喜爱阅读的同学发现,化学课本中的图表资料可以为我们提供很多信息.
表一:部分酸、碱和盐的溶解性表(20℃)
表二:部分法定计量单位
①Ⅰ处物质的名称是硫酸亚铁,该物质溶(填“溶”或“不溶”)于水.
②Ⅱ处“量的名称”是物质的量,Ⅲ处“单位符号”是g/mol.
表一:部分酸、碱和盐的溶解性表(20℃)
| 氢氧根和酸根 原子和原子团 | $\stackrel{-1}{OH}$ | $\stackrel{-2}{S{O}_{4}}$ |
| … | … | … |
| $\stackrel{+2}{Fe}$ | 不 | Ⅰ |
| … | … | … |
| 量的名称 | 量的符号 | 单位名称 | 单位符号 | 备注 |
| … | … | … | … | … |
| Ⅱ | n | … | mol | … |
| 摩尔质量 | M | … | Ⅲ | … |
②Ⅱ处“量的名称”是物质的量,Ⅲ处“单位符号”是g/mol.
14.在Cu(NO3)2和AgNO3的混合溶液中加入一定量的Zn,充分反应后过滤,留在滤纸上的固体一定( )
| A. | 有Zn | B. | 有ZnCuAg | C. | 有Cu和Ag | D. | 有Ag |

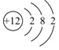 ,镁元素位于周期表中第三周期.;
,镁元素位于周期表中第三周期.;