题目内容
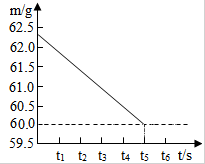 将碳酸钠和硫酸钠的固体混合物20g,放入烧杯中,再加入过量的稀硫酸220.4克,充分反应,无气体产生时,所得溶液质量为236克,反应的时间(t)和烧杯及其所盛物质总质量(m)的关系如图所示:
将碳酸钠和硫酸钠的固体混合物20g,放入烧杯中,再加入过量的稀硫酸220.4克,充分反应,无气体产生时,所得溶液质量为236克,反应的时间(t)和烧杯及其所盛物质总质量(m)的关系如图所示:(1)求20g固体混合物中硫酸钠的质量分数.
(2)求所得溶液的溶质质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钠的质量、生成硫酸钠的质量,进一步可以计算20g固体混合物中硫酸钠的质量分数和所得溶液的溶质质量分数.
解答:解:(1)设碳酸钠的质量为x,生成硫酸钠的质量为y,
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑,
106 142 44
x y 20g+220.4g-236g
=
=
,
x=10.6g,y=14.2g,
20g固体混合物中硫酸钠的质量分数为:
×100%=47%,
答:20g固体混合物中硫酸钠的质量分数为47%.
(2)所得溶液的溶质质量分数为:
×100%=10%,
答:所得溶液的溶质质量分数为10%.
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑,
106 142 44
x y 20g+220.4g-236g
| 106 |
| x |
| 142 |
| y |
| 44 |
| 20g+220.4g-236g |
x=10.6g,y=14.2g,
20g固体混合物中硫酸钠的质量分数为:
| 20g-10.6g |
| 20g |
答:20g固体混合物中硫酸钠的质量分数为47%.
(2)所得溶液的溶质质量分数为:
| 20g-10.6g+14.2g |
| 236g |
答:所得溶液的溶质质量分数为10%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
下列有关与稀盐酸发生的化学变化中,不属于复分解反应的是( )
| A、HCl+NaOH=NaCl+H2O |
| B、Fe+2HCl=FeCl2+H2↑ |
| C、HCl+AgNO3=AgCl↓+HNO3 |
| D、2HCl+Na2CO3=2NaCl+H2O+CO2↑ |

 表示氨原子,●表示氧原子,○表示氢原子;各物质未配平).请分析在该反应中参加反应的NH3与O2的分子个数之比为
表示氨原子,●表示氧原子,○表示氢原子;各物质未配平).请分析在该反应中参加反应的NH3与O2的分子个数之比为