题目内容
菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究.取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收.NaOH溶液增加的质量记录如下表:
说明:菱镁矿中的杂质不溶于水,不与酸发生反应.
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为 .
(2)计算该菱镁矿中镁元素的质量分数.(写出计算过程)
(3)该实验研究中所用H2SO4溶液的溶质的质量分数是 .
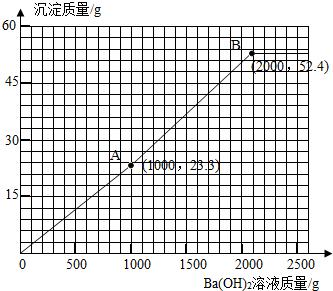
(4)为避免溶液排放对环境的影响,某同学对上述反应后溶液进行了过滤,并在滤液中加入了1.71%的Ba(OH)2溶液.请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图.(作图,并标出曲线折点的坐标)
| 加入H2SO4溶液的质量/g | 50 | 100 | 150 | 200 |
| NaOH溶液增加的质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为
(2)计算该菱镁矿中镁元素的质量分数.(写出计算过程)
(3)该实验研究中所用H2SO4溶液的溶质的质量分数是
(4)为避免溶液排放对环境的影响,某同学对上述反应后溶液进行了过滤,并在滤液中加入了1.71%的Ba(OH)2溶液.请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图.(作图,并标出曲线折点的坐标)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据表中信息可知生成CO2的质量;
(2)结合化学方程式根据二氧化碳的质量计算出碳酸镁的质量,进而即可计算出镁元素的质量分数;
(3)结合化学方程式和表中信息根据二氧化碳的质量即可解答;
(4)依据化学反应中元素守恒,有硫酸中硫酸根离子的质量,可计算出生沉淀的质量,和消耗氢氧化钡的质量;找到曲线折点即可画图.
(2)结合化学方程式根据二氧化碳的质量计算出碳酸镁的质量,进而即可计算出镁元素的质量分数;
(3)结合化学方程式和表中信息根据二氧化碳的质量即可解答;
(4)依据化学反应中元素守恒,有硫酸中硫酸根离子的质量,可计算出生沉淀的质量,和消耗氢氧化钡的质量;找到曲线折点即可画图.
解答:解:(1)表中信息可知10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为4.4g;
(2)设菱镁矿中MgCO3的质量为x,所用H2SO4溶液的溶质的质量分数是y,生成MgSO4的质量为z;
MgCO3+H2SO4=MgSO4+H2O+CO2↑
84 98 120 44
x 100g?y z 4.4g
=
,
x=8.4g,y=9.8%,z=12g
菱镁矿中镁元素的质量分数:
×100%=24%;
(3)
=
y=9.8%
(4)①加入的氢氧化钡可先与过量的稀硫酸反应.由于过量的稀硫酸中硫酸的质量为(200g-100g)×9.8%=9.8g.设和H2SO4反应生成的硫酸钡为m,消耗的Ba(OH)2为n,
H2SO4+Ba(OH)2=BaSO4↓+H2O
98 171 233
9.8g n m
=
m=23.3g n=17.1g
则该阶段消耗的氢氧化钡溶液的质量=
×100%=1000g,
所以图象中的第一个折点的坐标为A(1000,23.3).
②再加入的氢氧化钡与硫酸镁反应.设和MgSO4+反应生成的硫酸钡的质量为a,生成的Mg(OH)2质量为b,
MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓
120 171 233 58
12g a b c
a=17.1g,b=23.g,c=5.8g
则这一阶段消耗的氢氧化钡溶液的质量=
×100%=1000g,
因此图象中的第二个折点所用的氢氧化钡溶液的质量为1000g+1000g=2000g.同时沉淀的质量为23.3g+23.3g+5.8g=52.4 g.所以图象中的第二个折点的坐标为B(2000,52.4).
③再加入氢氧化钡时,不再产生沉淀.
作图见下图曲线:
答案:(1)4.4g;
(2)菱镁矿中镁元素的质量分数是24%;
(3)所用H2SO4溶液的溶质的质量分数是9.8%;
(4)作图见右图曲线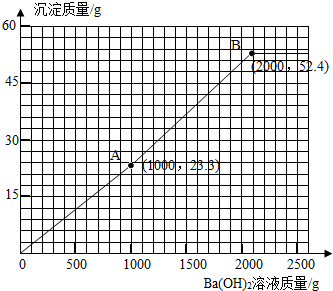
(2)设菱镁矿中MgCO3的质量为x,所用H2SO4溶液的溶质的质量分数是y,生成MgSO4的质量为z;
MgCO3+H2SO4=MgSO4+H2O+CO2↑
84 98 120 44
x 100g?y z 4.4g
| 84 |
| x |
| 44 |
| 4.4g |
x=8.4g,y=9.8%,z=12g
菱镁矿中镁元素的质量分数:
8.4g×
| ||
| 10g |
(3)
| 98 |
| 100g?y |
| 44 |
| 4.4g |
y=9.8%
(4)①加入的氢氧化钡可先与过量的稀硫酸反应.由于过量的稀硫酸中硫酸的质量为(200g-100g)×9.8%=9.8g.设和H2SO4反应生成的硫酸钡为m,消耗的Ba(OH)2为n,
H2SO4+Ba(OH)2=BaSO4↓+H2O
98 171 233
9.8g n m
| 98 |
| 9.8g |
| 233 |
| x |
则该阶段消耗的氢氧化钡溶液的质量=
| 17.1 |
| 1.71% |
所以图象中的第一个折点的坐标为A(1000,23.3).
②再加入的氢氧化钡与硫酸镁反应.设和MgSO4+反应生成的硫酸钡的质量为a,生成的Mg(OH)2质量为b,
MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓
120 171 233 58
12g a b c
a=17.1g,b=23.g,c=5.8g
则这一阶段消耗的氢氧化钡溶液的质量=
| 17.1 |
| 1.71% |
因此图象中的第二个折点所用的氢氧化钡溶液的质量为1000g+1000g=2000g.同时沉淀的质量为23.3g+23.3g+5.8g=52.4 g.所以图象中的第二个折点的坐标为B(2000,52.4).
③再加入氢氧化钡时,不再产生沉淀.
作图见下图曲线:

答案:(1)4.4g;
(2)菱镁矿中镁元素的质量分数是24%;
(3)所用H2SO4溶液的溶质的质量分数是9.8%;
(4)作图见右图曲线

点评:本题是一道综合性很强的根据化学方程式计算,只要找准已知量和相应未知量是解答此类题目的关键所在,关于作图要找准起始点和折点即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
氧化镁,氢氧化镁和碳酸镁组成的混合物10g,向其中加入一定量溶质质量分数为20%的稀盐酸恰好完全反应,再向反应后的溶液中加入适量的NaOH溶液,完全反应后得到11.6g沉淀,则原混合物中镁元素的质量分数为( )
| A、10% | B、24% |
| C、12% | D、48% |
下列对CO2的功过是非评价错误的是( )
| A、二氧化碳和一氧化碳一样都是空气污染物 |
| B、二氧化碳常被压缩冲入水中以制取各类碳酸饮料 |
| C、温室效应为人类提供了适宜的生存温度 |
| D、CO2参加光合作用可提高农作物的产量 |
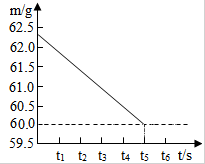 将碳酸钠和硫酸钠的固体混合物20g,放入烧杯中,再加入过量的稀硫酸220.4克,充分反应,无气体产生时,所得溶液质量为236克,反应的时间(t)和烧杯及其所盛物质总质量(m)的关系如图所示:
将碳酸钠和硫酸钠的固体混合物20g,放入烧杯中,再加入过量的稀硫酸220.4克,充分反应,无气体产生时,所得溶液质量为236克,反应的时间(t)和烧杯及其所盛物质总质量(m)的关系如图所示:
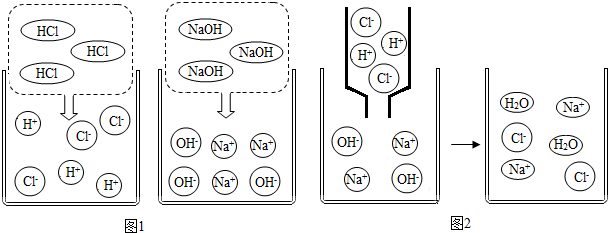
 某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰.该小组同学进行如下探究:
某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰.该小组同学进行如下探究: