题目内容
7.已知反应Fe+2FeCl3═3FeCl2 Cu+2FeCl3═2FeCl2+CuCl2,在氯化铁和氯化铜的混合溶液中,加入过量的铁粉,若充分反应后溶液的质量没有改变.则原混合溶液中Fe3+和Cu2+的个数比为( )| A. | 14:5 | B. | 5:14 | C. | 7:2 | D. | 2:7 |
分析 根据在氯化铁和氯化铜的混合溶液中,加入过量的铁粉,发生的反应是:Fe+2FeCl3═3FeCl2,Cu+2FeCl3═2FeCl2+CuCl2,Fe+CuCl2=FeCl2+Cu,充分反应后溶液的质量没有改变,所以反应后得到的固体残渣的质量与参加反应的铁的质量相等,则消耗的铁的质量等于生成的铜的质量进行分析.
解答 解:设混合物中含有xmol氯化铁,ymol氯化铜,在氯化铁和氯化铜的混合溶液中,加入过量的铁粉,发生的反应为:
Fe+2FeCl3═3FeCl2,
1 2
$\frac{1}{2}x$ x
Fe+CuCl2=FeCl2+Cu
1 1 1
y y y
充分反应后溶液的质量没有改变,所以反应后得到的固体残渣的质量与参加反应的铁的质量相等,则消耗的铁的质量等于生成的铜的质量
所以(0.5x+y)×56=64y
x:y=2:7
所以原混合溶液中Fe3+和Cu2+的个数比为:2:7.
故选:D.
点评 本题主要考查了铁离子与亚铁离子之间的转化、混合物的计算,注意把握化学方程式的书写,依据质量关系结合化学方程式计算,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.除去下列物质中的杂质所选用的试剂及操作方法正确的一组是( )
| 选项 | 物 质 | 所加试剂 | 操作方法 |
| A | KOH溶液(K2CO3) | 适量Ba(OH)2溶液 | 过滤 |
| B | O2气体(N2) | 铜网 | 将气体缓缓通过灼热的足量铜网 |
| C | HCl溶液(BaCl2) | 足量稀硫酸 | 过滤、洗涤、干燥 |
| D | FeSO4(CuSO4) | 足量蒸馏水、金属铁 | 过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
15.下列装置或操作正确的是( )
| A. |  5mL稀氢氧化钠溶液 | B. | 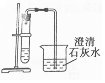 石灰石与盐酸反应 | ||
| C. |  用澄清石灰水检验 | D. |  液体的量取 |
12.2013年12月份,全国多地出现严重的雾霾天气.关心环境,呼吸清洁的空气是国人的共识.下列关于空气污染和防治的认识错误的是( )
| A. | 工业废气、燃料不完全燃烧、汽车尾气都会导致雾霾天气的形成 | |
| B. | 城市限制小汽车的购买和使用是治理雾霾天气的最佳方案 | |
| C. | 可吸入颗粒物、二氧化硫、一氧化碳都是空气污染指数的检测项目 | |
| D. | 加强对空气质量的监测也是保护空气的重要手段 |
1.在下列概念中,一定属于化学变化的是( )
| A. | 光合作用 | B. | 液化 | C. | 溶解 | D. | 爆炸 |
2. 有一种石灰石样品的主要成分是CaCO3.课外小组同学将100g稀盐酸分5次加入到35g石灰石样品中(已知杂质不与盐酸反应也不溶于水),得到如下部分数据和图象.请仔细观察下列表格和图象计算:
有一种石灰石样品的主要成分是CaCO3.课外小组同学将100g稀盐酸分5次加入到35g石灰石样品中(已知杂质不与盐酸反应也不溶于水),得到如下部分数据和图象.请仔细观察下列表格和图象计算:
计算:
(1)a的值为25克;
(2)所用盐酸的溶质质量分数18.25%.
(3)恰好完全反应后所得溶液的溶质质量分数24.4%(结果精确到0.1%);
(4)10%的CaCl2溶液可作为路面保湿剂.欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰右粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计).
 有一种石灰石样品的主要成分是CaCO3.课外小组同学将100g稀盐酸分5次加入到35g石灰石样品中(已知杂质不与盐酸反应也不溶于水),得到如下部分数据和图象.请仔细观察下列表格和图象计算:
有一种石灰石样品的主要成分是CaCO3.课外小组同学将100g稀盐酸分5次加入到35g石灰石样品中(已知杂质不与盐酸反应也不溶于水),得到如下部分数据和图象.请仔细观察下列表格和图象计算:| 次数 | 1 | 2 | 3 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(1)a的值为25克;
(2)所用盐酸的溶质质量分数18.25%.
(3)恰好完全反应后所得溶液的溶质质量分数24.4%(结果精确到0.1%);
(4)10%的CaCl2溶液可作为路面保湿剂.欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰右粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计).






 和
和 与反应后生成的
与反应后生成的 各粒子间的个数比为2:1:2.
各粒子间的个数比为2:1:2.