题目内容
完成下列化学方程式□Fe2O3+□CO═□Fe+□CO2□CH3CH2OH+□O2═□CO2+□H2O
□Al+□H2SO4═□Al2(SO4)3+□H2↑□Na+□H2O═□NaOH+□H2↑
【答案】分析:配平化学方程式的关键是等号两边各原子的种类与数目必须相等,在方程式中出现的原子团要看成一个整体,不能拆开,用最小公倍数法再结合观察法即可一一配平.
解答:解:根据Fe2O3中氧原子的数目进行配平,CO与CO2前面的化学计量数与Fe2O3中氧原子的数目相等,故答案为:Fe2O3+3CO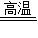 2Fe+3CO2;
2Fe+3CO2;
氧元素的原子在右端的总数是一奇一偶,选定氧元素作为配平的起点,把奇数乘以2先变化为偶数,即先把H2O中的氧原子数先变为偶数,然后再依次配平其他元素的原子.最后分别加上合适的反应条件,故答案为:C2H5OH+3O2 2CO2+3H2O;
2CO2+3H2O;
等号前1个SO42-,一个Al,等号后有3个SO42-,2个Al,所以在Al前配2,在H2SO4前配3,再观察可知H2前配3即可,故答案为:2Al+3H2SO4=Al2(SO4)3+3H2↑;
可以用观察法来配平,选定氢元素作为配平的起点,然后再依次配平其他元素的原子,故答案为:2Na+2H2O═2NaOH+H2↑.
点评:本题主要考查了质量守恒定律方面的知识,利用质量守恒定律配平化学方程式,化学反应前后元素的种类和原子的个数不变.
解答:解:根据Fe2O3中氧原子的数目进行配平,CO与CO2前面的化学计量数与Fe2O3中氧原子的数目相等,故答案为:Fe2O3+3CO
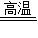 2Fe+3CO2;
2Fe+3CO2;氧元素的原子在右端的总数是一奇一偶,选定氧元素作为配平的起点,把奇数乘以2先变化为偶数,即先把H2O中的氧原子数先变为偶数,然后再依次配平其他元素的原子.最后分别加上合适的反应条件,故答案为:C2H5OH+3O2
 2CO2+3H2O;
2CO2+3H2O;等号前1个SO42-,一个Al,等号后有3个SO42-,2个Al,所以在Al前配2,在H2SO4前配3,再观察可知H2前配3即可,故答案为:2Al+3H2SO4=Al2(SO4)3+3H2↑;
可以用观察法来配平,选定氢元素作为配平的起点,然后再依次配平其他元素的原子,故答案为:2Na+2H2O═2NaOH+H2↑.
点评:本题主要考查了质量守恒定律方面的知识,利用质量守恒定律配平化学方程式,化学反应前后元素的种类和原子的个数不变.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
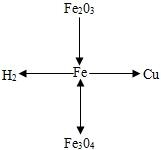 化学上通常用“→”表示物质能向箭头所指示方向转化、用“←→”表示箭头两端物质之间在一定条件下可以相互转化,从而将许多物质之间的关系用简单的网络图表示出来(如示例).
化学上通常用“→”表示物质能向箭头所指示方向转化、用“←→”表示箭头两端物质之间在一定条件下可以相互转化,从而将许多物质之间的关系用简单的网络图表示出来(如示例).