��Ŀ����
��2011?������ģ�⣩��ͼ��A��B���ֹ������ʵ��ܽ�����¶ȱ仯�����ߣ���ش���1����ʱ��A��B�����ʵ��ܽ����ȣ�
��2��50��ʱ����A��B��15g�ֱ�ӵ���ʢ��50gˮ����ֻС�ձ��У���ֽ����������ʣ�ࣨ�A����B��������һ�������ٻ���ӿ˲��ܴﵽ����״̬��
��3������40��ʱA���ʵIJ�������Һ���ڲ��������ʵ�����£���ʹ���ɱ�����Һ�����д�ʩ��ʵ�ֵ��ǣ�����ţ���
�����¶Ȣ������¶Ȣ������ܼ����������ܼ���
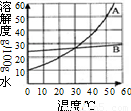
���𰸡����������ܽ�����߿��ԣ����A��B�����ʵ��ܽ�����߽���һ���Ӧ���¶ȣ���50��ʱ��A��B���ܽ�ȴ�С�������ж�A��B��15g�ֱ�ӵ�50gˮ���ܷ�ȫ���ܽ⣻��A���ܽ�������¶ȵ����ߵı仯���ƣ�����ȷ����A���ʵIJ�������Һ��ɱ�����Һ���Բ�ȡ�ķ�����
����⣺��1�����ܽ�����߿��Կ�����30��ʱ��A��B�����ʵ��ܽ�����߽���һ�㣬A��B�����ʵ��ܽ����ȣ�
��2��50��ʱ��A���ܽ��Ϊ50g��B���ܽ��С��30g���ʽ�A��B��15g�ֱ�ӵ���ʢ��50gˮ����ֻС�ձ��У���ֽ����A��ȫ���ܽ⣬B��ʣ�ࣻ���¶���50gˮ�У�����ܽ�A25g�������ٻ����10g���ܴﵽ����״̬��
��3��A���ܽ�������¶ȵ����߶�����40��ʱA���ʵIJ�������Һ���ڲ��������ʵ�����£���ʹ���ɱ�����Һ�����Բ�ȡ�����¶ȡ������ܼ��ȷ�����
�ʴ�Ϊ����1��30����2��B��10����3����
�����������ѶȲ�����Ҫ�����˹����ܽ����������ʾ�����壬ͨ��������Լ�ǿѧ���Թ����ܽ�ȵ����⣬����ѧ��Ӧ��֪ʶ��������������
����⣺��1�����ܽ�����߿��Կ�����30��ʱ��A��B�����ʵ��ܽ�����߽���һ�㣬A��B�����ʵ��ܽ����ȣ�
��2��50��ʱ��A���ܽ��Ϊ50g��B���ܽ��С��30g���ʽ�A��B��15g�ֱ�ӵ���ʢ��50gˮ����ֻС�ձ��У���ֽ����A��ȫ���ܽ⣬B��ʣ�ࣻ���¶���50gˮ�У�����ܽ�A25g�������ٻ����10g���ܴﵽ����״̬��
��3��A���ܽ�������¶ȵ����߶�����40��ʱA���ʵIJ�������Һ���ڲ��������ʵ�����£���ʹ���ɱ�����Һ�����Բ�ȡ�����¶ȡ������ܼ��ȷ�����
�ʴ�Ϊ����1��30����2��B��10����3����
�����������ѶȲ�����Ҫ�����˹����ܽ����������ʾ�����壬ͨ��������Լ�ǿѧ���Թ����ܽ�ȵ����⣬����ѧ��Ӧ��֪ʶ��������������

��ϰ��ϵ�д�
 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д�
�����Ŀ
��2011?������һģ��������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�
��1��Na2CO3�ܽ������Ϊ���a����b������
��2��Ҫ��ȥNa2CO3�����е�����NaHCO3��Ӧ���õ����������ǣ���д��ţ���
����ȴ�ȱ�����Һ �������ܼ� ���ܽ����
��3����֪Na2CO3ת��ΪNaHCO3�ķ�ӦΪNa2CO3+CO2+H2O��2NaHCO3������������Ϣ��Ҫ��ȥNaHCO3������Һ�е�����Na2CO3��Ӧ���õĻ�ѧ�����ǣ�
��4��40��ʱ��100g Na2CO3�ı�����Һ�к���g���ʣ�����Һ��������������Ϊ%������������ȷ��0.1��
��5������30%��̼������Һ100g��ϡ�͵�10%����Ҫ��ˮmL��
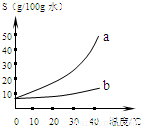
��1��Na2CO3�ܽ������Ϊ���a����b������
| 0�� | 10�� | 20�� | 30�� | 40�� | |
| Na2CO3���ܽ�ȣ�g/100gˮ�� | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3���ܽ�ȣ�g/100gˮ�� | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
����ȴ�ȱ�����Һ �������ܼ� ���ܽ����
��3����֪Na2CO3ת��ΪNaHCO3�ķ�ӦΪNa2CO3+CO2+H2O��2NaHCO3������������Ϣ��Ҫ��ȥNaHCO3������Һ�е�����Na2CO3��Ӧ���õĻ�ѧ�����ǣ�
��4��40��ʱ��100g Na2CO3�ı�����Һ�к���g���ʣ�����Һ��������������Ϊ%������������ȷ��0.1��
��5������30%��̼������Һ100g��ϡ�͵�10%����Ҫ��ˮmL��



