题目内容
5.下列实验现象的描述中,正确的是( )| A. | 紫色石蕊溶液中通入二氧化碳,会变成红色 | |
| B. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| C. | 打开装有浓盐酸试剂瓶的瓶塞,瓶口上方有白烟产生 | |
| D. | 木炭在氧气中燃烧发出白光,生成二氧化碳 |
分析 A、根据二氧化碳的化学性质,进行分析判断.
B、根据铁丝在空气中不能燃烧,进行分析判断.
C、根据浓盐酸具有挥发性,进行分析判断.
D、根据木炭在氧气中燃烧的现象进行分析判断.
解答 解:A、紫色石蕊溶液中通入二氧化碳,二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊溶液变红色,故选项说法正确.
B、铁丝在空气中只能烧至发红,不会产生火星,故选项说法错误.
C、浓盐酸具有挥发性,打开装有浓盐酸试剂瓶的瓶塞,瓶口上方有白雾产生,故选项说法错误.
D、木炭在氧气中燃烧发出白光,生成二氧化碳是实验结论而不是实验现象,故选项说法错误.
故选:A.
点评 本题难度不大,掌握二氧化碳的化学性质、常见物质燃烧的现象、浓盐酸具有挥发性等即可正确解答,在描述实验现象时,需要注意烟和雾、实验结论和实验现象的区别.

练习册系列答案
相关题目
20.为了研究物质的溶解现象,设计并进行了如下实验,下列说法不正确的是( )
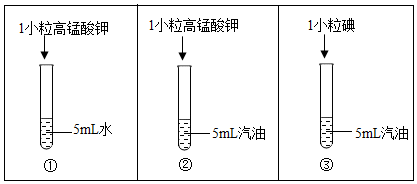

| A. | 实验①中的固体溶解,形成紫红色溶液;实验②中的固体几乎不溶解 | |
| B. | 设计实验②、③的目的是比较高锰酸钾和碘在汽油中溶解情况 | |
| C. | 对比实验①、②可得出的结论是高锰酸钾在水中的溶解性比汽油中的好 | |
| D. | 实验说明不同物质在同一溶剂中溶解性是相同的,同一种物质在不同溶剂中溶解性也是相同的 |
10.下列化学用语解说正确的是( )
| A. | Fe2+:表示1个铁离子带2个正电荷 | B. | $\begin{array}{l}+2\\ Mg\end{array}$:+2价的镁原子 | ||
| C. | 2P:2个磷分子 | D. | O2:氧气 |
17.用氢气还原氧化铜的方法测定某氧化铜样品的纯度(氢气和一氧化碳化学性质相似,有还原性,杂质不与氢气反应),同学们设计了如图所示实验装置,准确称取20克干燥样品进行实验.
(1)在实验中,乙装置的作用是检验氢气中的水蒸气是否除尽.
(2)准确称取完全反应前后装置丙和丁的质量如表:
小明同学想根据装置丁求出氧化铜样品的纯度,请同学们帮助他(写出计算过程).
(3)请分析,选择装置丙的数据比装置丁的数据进行计算求氧化铜的纯度的更合理的原因是装置丁中增加的质量包括反应生成的水的质量和浓硫酸吸收的空气中的水蒸气的质量.
(4)假设丙装置反应前质量为m,充分反应后质量为n,装置丁的质量反应前为a,反应后为b,请用m、n、a、b的代数式表示水中氢氧元素质量比$\frac{b-a-m+n}{m-n}$.(不考虑其它影响因素)

(1)在实验中,乙装置的作用是检验氢气中的水蒸气是否除尽.
(2)准确称取完全反应前后装置丙和丁的质量如表:
| 装置丙 | 装置丁 | |
| 反应前 | 48.8克 | 161.2克 |
| 反应后 | 45.6克 | 164.98克 |
(3)请分析,选择装置丙的数据比装置丁的数据进行计算求氧化铜的纯度的更合理的原因是装置丁中增加的质量包括反应生成的水的质量和浓硫酸吸收的空气中的水蒸气的质量.
(4)假设丙装置反应前质量为m,充分反应后质量为n,装置丁的质量反应前为a,反应后为b,请用m、n、a、b的代数式表示水中氢氧元素质量比$\frac{b-a-m+n}{m-n}$.(不考虑其它影响因素)
14.如图表示四种物质的分子模型,下列有关说法中正确的是( )


| A. | 物质甲是单质,其相对分子质量为2g | |
| B. | 物质乙是相对分子质量最小的氧化物,其中氧元素与氢元素的质量比为1:2 | |
| C. | 物质丙、丁虽然分子模型示意图不相同,但相对分子质量相同 | |
| D. | 物质丙中氧元素质量分数最大,物质丁的分子中C、H原子个数比为1:3 |
15.下列实验现象的描述错误的是( )
| A. | 铁丝在氧气中燃烧火星四射 | |
| B. | 将CO2气体通入石蕊溶液中,溶液变红 | |
| C. | 木炭在氧气中燃烧发出淡蓝色火焰 | |
| D. | 生锈的铁钉放入稀盐酸中,溶液由无色变黄色 |
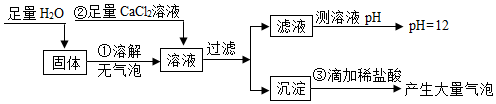
 结合如图中KNO3、NaCl两种固体物质的溶解度曲线回答下列问题
结合如图中KNO3、NaCl两种固体物质的溶解度曲线回答下列问题