题目内容
2.过氧化钠(Na2O2)是一种淡黄色的固体,它能与CO2、H2O反应,其化学方程式为:2Na2O2+2CO2═2Na2CO3+O2,2Na2O2+2H2O═4NaOH+O2↑.为探究实验室敞口放置的过氧化钠中固体的成分,该小组同学进行了如下实验,请回答下列问题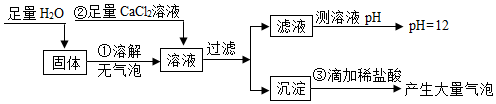
(1)由步骤①中的实验现象可得出什么结论?
(2)步骤②中所加试剂的目的是什么?
(3)根据实验判断敞口放置的过氧化钠中固体的成分是什么?
分析 加入水时,不产生气泡,说明固体中不含有过氧化钠;
碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
碳酸钠溶液和氢氧化钠溶液都是显碱性的溶液,都能使酚酞试液变红色.
解答 解:(1)步骤①中,加入足量水后,不产生气泡,说明固体中不含有过氧化钠;
(2)步骤②中,加入足量的氯化钙溶液,既能够检验碳酸钠,又能够除去碳酸钠,以免影响对氢氧化钠的检验;
(3)步骤①中,加入足量水后,不产生气泡,说明固体中不含有过氧化钠,加入氯化钙溶液后产生白色沉淀,说明固体中含有碳酸钠,滤液的pH=12,说明溶液显碱性,进一步说明固体中含有氢氧化钠.
故答案为:固体中不含有过氧化钠;检验并且除去碳酸钠;碳酸钠和氢氧化钠.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
12.下列对有关主题知识的归纳错误的是( )
| A、环保与物质的利用 减少白色污染--使用可降解塑料 玉米叶色淡黄--可施加硝酸铵改善 | B、元素与人体健康 人体缺铁--易引起贫血 人体缺氟--易产生龋齿 |
| C、生活常识 洗涤剂洗去油污--乳化作用 煤炉取暖防中毒--开窗通风 | D、安全常识 室内煤气泄漏--立即打开排风扇 浓硫酸沾到皮肤上--立即用水清洗 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
5.下列实验现象的描述中,正确的是( )
| A. | 紫色石蕊溶液中通入二氧化碳,会变成红色 | |
| B. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| C. | 打开装有浓盐酸试剂瓶的瓶塞,瓶口上方有白烟产生 | |
| D. | 木炭在氧气中燃烧发出白光,生成二氧化碳 |
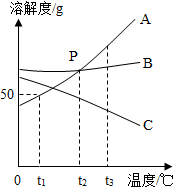 A、B、C三种固体物质的溶解度曲线如图所示,回答下列问题
A、B、C三种固体物质的溶解度曲线如图所示,回答下列问题