题目内容
有一包白色粉末可能由Na2SO4、Na2CO3、BaCl2、CuSO4中的一种或几种组成.小刚为了测定该白粉末的组成,设计了如图所示实验:
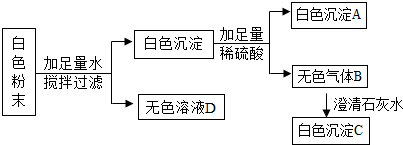
请你根据如图实验现象帮助小刚判断:
(1)白色沉淀A是 ,白色粉末中一定不含有 ,肯定含有 .
(2)写出B→C的化学方程式 .

请你根据如图实验现象帮助小刚判断:
(1)白色沉淀A是
(2)写出B→C的化学方程式
考点:物质的鉴别、推断,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:混合物组成的推断题
分析:(1)根据铜离子在溶液中显蓝色,碳酸钡沉淀会溶于酸,硫酸钡沉淀不会溶于酸进行分析;
(2)根据(1)中推出的反应物、生成物书写方程式.
(2)根据(1)中推出的反应物、生成物书写方程式.
解答:解:(1)依据图框可知:白色粉末加水后会生成无色液体和白色沉淀,说明一定不存在硫酸铜,无色气体B和澄清石灰水会生成白色沉淀C,所以B就是二氧化碳,C就是碳酸钙,白色沉淀和硫酸反应会生成二氧化碳和沉淀,但是硫酸会引入硫酸根离子,所以白色沉淀中一定有碳酸钡,硫酸钡不能确定,所以混合物中一定存在碳酸钠和氯化钡,不能确定硫酸钠的存在,
故答案为:BaSO4;CuSO4;Na2CO3、BaCl2
(2)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,故答案为:CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:
(1)BaSO4;CuSO4;Na2CO3、BaCl2;(2)CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:BaSO4;CuSO4;Na2CO3、BaCl2
(2)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,故答案为:CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:
(1)BaSO4;CuSO4;Na2CO3、BaCl2;(2)CO2+Ca(OH)2=CaCO3↓+H2O.
点评:在解此类题时,首先分析混合物中各物质的性质,然后结合题中的现象进行分析混合物的成分.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应中不属于复分解反应的是( )
| A、H2SO4+Ca(OH)2=CaSO4+2H2O |
| B、H2SO4+BaCl=BaSO4↓+2HCl |
| C、2HCl+Fe=FeCl2+H2↑ |
| D、2HCl+NaOH=NaCl+CO2↑+2H2O |
下列不能体现化学作用的是( )
| A、海水淡化和水污染的防治 |
| B、火车提速和提高公路的运输能力 |
| C、研制新型塑料,减少“白色污染” |
| D、研制新型药物,提高人类战胜疾病的能力 |
将下列物质分别按混合物、纯净物、单质、化合物分类正确的一组是( )
①空气 ②氧气 ③水蒸气 ④高锰酸钾 ⑤铁粉 ⑥氮气
①空气 ②氧气 ③水蒸气 ④高锰酸钾 ⑤铁粉 ⑥氮气
| 混合物 | 纯净物 | 单质 | 化合物 | |
| A | ①③ | ②⑤⑥ | ② | ④ |
| B | ①②⑤⑥ | ③④ | ②⑤ | ①③④ |
| C | ① | ②③④⑤⑥ | ②⑤⑥ | ③④ |
| D | ①③④ | ②⑤⑥ | ⑤⑥ | ①③④ |
| A、A | B、B | C、C | D、D |
下列说法正确的是( )
| A、溶液一定呈现液态 |
| B、当水分不蒸发时,溶液不管放置多久,溶质也不会分离出来 |
| C、均一、稳定、透明的液体不一定是溶液 |
| D、溶液中的溶剂都是水 |
下列实验现象描述正确的是( )
| A、铁粉加入到稀盐酸中:银白色固体表面产生气泡,固体减少,放热,溶液由无色变为浅绿色 |
| B、镁在空气中燃烧:发出强光,放出热量,产生大量的白雾 |
| C、向硫酸铜溶液中加入铁钉:铁钉表面覆盖一层白色物质,溶液变成浅绿色 |
| D、“假黄金”(铜锌合金)灼烧:黄色会变黑 |
