题目内容
17.小林在初二科学课上学习了氧气的实验室制法后,想用其他方法制取氧气.他请教老师后,决定用二氧化碳和过氧化钠(Na2O2)反应来制取氧气,其实验装置如图所示:
(1)该反应的另一种产物是纯碱,写出上述反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2↑.
(2)C装置中澄清石灰水的作用是检验二氧化碳是否除尽.
分析 (1)二氧化碳通过A装置反应生成碳酸钠和氧气.
(2)二氧化碳通过A装置并不能反应完,通过B装置除去未反应的二氧化碳,C装置用来检验二氧化碳是否除干净,以确保收集到纯净的氧气.故答案为:检验二氧化碳是否除尽.
解答 解:(1)二氧化碳通过A装置反应生成碳酸钠和氧气.故答案为:2Na2O2+2CO2=2Na2CO3+O2↑.
(2)二氧化碳通过A装置并不能反应完,通过B装置除去未反应的二氧化碳,C装置用来检验二氧化碳是否除干净,以确保收集到纯净的氧气.故答案为:检验二氧化碳是否除尽.
答案:
(1)2Na2O2+2CO2=2Na2CO3+O2↑.
(2)检验二氧化碳是否除尽.
点评 本题难度不大,主要考查气体的检验及气体的除杂等有关知识.

练习册系列答案
相关题目
8.通过观察实验现象获得证据,从而归纳出相关结论是科学上常用的研究方法,下列实验现象和对应的结论正确的是( )
| A. | 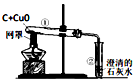 试管①红色粉末变成黑色,试管②的澄清石灰水变浑浊,说明碳具有还原性 | |
| B. |  铁丝表面覆盖红色物质,溶液由蓝色逐渐变成无色,说明铁的金属活动性强于铜 | |
| C. |  烧杯中的红色溶液逐渐变浅最后变成无色,说明盐酸与氢氧化钠能发生反应 | |
| D. | 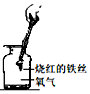 铁丝在氧气中剧烈燃烧、火星四射,生成的黑色物质是氧化铁 |
12.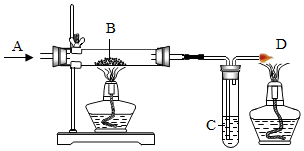 小陈利用如图所示装置进行气体性质的探究实验.A处通入无色气体(可能是H2或CO);B处玻璃管中盛放黑色粉末CuO,C处试管中盛放澄清石灰水溶液.
小陈利用如图所示装置进行气体性质的探究实验.A处通入无色气体(可能是H2或CO);B处玻璃管中盛放黑色粉末CuO,C处试管中盛放澄清石灰水溶液.
(1)根据要求完成下表填写:
(2)实验Ⅰ通过B处的现象已能确定有铜这种产物,还需要在B与C之间加装一个装有无水硫酸铜(填药品名称)的干燥管,就能确定另一产物是水.
(3)实验Ⅱ、Ⅲ的D处导管尖嘴口需用酒精灯点燃的目的是把一氧化碳转化成二氧化碳,防止污染环境.
 小陈利用如图所示装置进行气体性质的探究实验.A处通入无色气体(可能是H2或CO);B处玻璃管中盛放黑色粉末CuO,C处试管中盛放澄清石灰水溶液.
小陈利用如图所示装置进行气体性质的探究实验.A处通入无色气体(可能是H2或CO);B处玻璃管中盛放黑色粉末CuO,C处试管中盛放澄清石灰水溶液.(1)根据要求完成下表填写:
| 序号 | 探究实验 | 简答 |
| Ⅰ | 若为H2与CuO的反应 | B处玻璃管观察到现象:出现水珠. |
| Ⅱ | 若为CO与CuO的反应 | B处反应的化学方程式:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2, 发生氧化反应的物质是:CO. |
| Ⅲ | 若为CO2与C 的反应 (B处换成酒精喷灯加热) | B处的黑色粉末逐渐减少,最后消失, D处观察到有蓝色的火焰. |
(3)实验Ⅱ、Ⅲ的D处导管尖嘴口需用酒精灯点燃的目的是把一氧化碳转化成二氧化碳,防止污染环境.
7.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥砂,可将粗盐溶于水,然后进行下列五项操作①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.下列操作顺序中最合适的是( )
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ⑤②④③① |

