题目内容
9. 电子产品的迅速发展离不开化学的重要贡献.如图是一款便携卷轴式太阳能手机充电器,其外壳由铝合金制成,铝合金属于金属材料.因其体积小巧轻便,适合户外运动携带,制造智能手机的关键材料有硅,工业上利用二氧化硅和碳在高温下制备单质硅,同时生成一种还原性气体,写出该反应的化学方程式SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.该反应的反应类型是置换反应,反应前后硅元素的化合价分别是+4价、0价.
电子产品的迅速发展离不开化学的重要贡献.如图是一款便携卷轴式太阳能手机充电器,其外壳由铝合金制成,铝合金属于金属材料.因其体积小巧轻便,适合户外运动携带,制造智能手机的关键材料有硅,工业上利用二氧化硅和碳在高温下制备单质硅,同时生成一种还原性气体,写出该反应的化学方程式SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.该反应的反应类型是置换反应,反应前后硅元素的化合价分别是+4价、0价.
分析 金属材料包括纯金属以及它们的合金;工业上利用二氧化硅和碳在高温下制备单质硅,同时生成一种还原性气体,由质量守恒定律,反应前后元素种类不变,该气体为一氧化碳,写出反应的化学方程式即可;单质中元素的化合价为0、在化合物中正负化合价代数和为零,结合含硅元素的化学式进行解答本题.
解答 解:铝合金属于合金,属于金属材料.
工业上利用二氧化硅和碳在高温下制备单质硅,同时生成一种还原性气体,由质量守恒定律,反应前后元素种类不变,该气体为一氧化碳,反应的化学方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
氧元素显-2价,设反应前二氧化硅中硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
根据单质中元素的化合价为0,Si属于单质,故硅元素的化合价为0.
故答案为:金属;SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;置换反应;+4价,0价.
点评 本题难度不大,掌握金属材料的范畴、化学方程式的书写方法、利用化合价的原则计算指定元素的化合价的方法等是正确解答本题的关键.

练习册系列答案
相关题目
19.下列四个化学方程式都表示酸与其他物质的反应,其中不能进行的是( )
| A. | 2HCl+Zn═ZnCl2+H2↑ | B. | 3H2SO4+Fe2O3═Fe2(SO4)3+3H2O | ||
| C. | HCl+NaNO3═NaCl+HNO3 | D. | HNO3+NaOH═NaNO3+H2O |
17. 小明家的大豆叶片边缘发黄(如图),且出现了倒伏现象.你认为应施用的肥料是( )
小明家的大豆叶片边缘发黄(如图),且出现了倒伏现象.你认为应施用的肥料是( )
 小明家的大豆叶片边缘发黄(如图),且出现了倒伏现象.你认为应施用的肥料是( )
小明家的大豆叶片边缘发黄(如图),且出现了倒伏现象.你认为应施用的肥料是( )| A. | Ca(H2PO4)2 | B. | NH4H2PO4 | C. | CO(NH2)2 | D. | KNO3 |
14.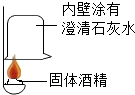 同学们在一次用餐中,对燃料“固体酒精”产生了好奇,于是对其成分进行探究.
同学们在一次用餐中,对燃料“固体酒精”产生了好奇,于是对其成分进行探究.
【查阅资料】
(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】
(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
【实验探究】
(1)按如图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论,此结论合理(选填“合理”或“不合理”).
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.写出产生白色沉淀化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl 过滤,取沉淀于试管中加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质的程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按如图探究.
②乙组认为甲组实验不能证明清液中一定有氢氧化钠,理由是Na2CO3溶液显碱性,也能是酚酞溶液变红.他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红.
【实验结论】经过讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是可完全除去Na2CO3,防止影响(或干扰)对NaOH的检验.
【扩展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC(填序号)
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液 D.Ba(NO3)2.
 同学们在一次用餐中,对燃料“固体酒精”产生了好奇,于是对其成分进行探究.
同学们在一次用餐中,对燃料“固体酒精”产生了好奇,于是对其成分进行探究.【查阅资料】
(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】
(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
【实验探究】
(1)按如图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论,此结论合理(选填“合理”或“不合理”).
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.写出产生白色沉淀化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl 过滤,取沉淀于试管中加稀盐酸,有气泡产生,写出产生气体的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质的程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按如图探究.
| 方案 | 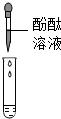 | 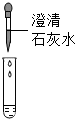 |
| 现象 | 溶液变红 | 产生产生白色沉淀 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
【实验结论】经过讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是可完全除去Na2CO3,防止影响(或干扰)对NaOH的检验.
【扩展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC(填序号)
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液 D.Ba(NO3)2.
19.从下列图片中不能获取的信息是( )


| A. | 分子之间有间隔 | |
| B. | 构成物质的粒子有分子、原子和离子 | |
| C. | 硅原子是由原子核和电子构成的 | |
| D. | 受热水分子运动速率加快 |
 常温下,过氧化氢(H2O2)溶液在二氧化锰的催化作用下能迅速分解生成氧气和水.现有下图所示的实验装置(分液漏斗可以通过调节活塞控制液体的流速)现用5%过氧化氢溶液制取氧气,请回答有关问题.
常温下,过氧化氢(H2O2)溶液在二氧化锰的催化作用下能迅速分解生成氧气和水.现有下图所示的实验装置(分液漏斗可以通过调节活塞控制液体的流速)现用5%过氧化氢溶液制取氧气,请回答有关问题. 空气是人类宝贵的自然资源.
空气是人类宝贵的自然资源.