题目内容
某石灰厂有一批石灰石原料,其中含有的杂质不与盐酸反应.为了测定该石灰石的纯度,兴趣小组的同学取用2g这种石灰石样品,并把20g稀盐酸分四次加入,充分反应后,经过滤、干燥等操作后,根据每次稀盐酸用量及剩余固体质量和实验数据绘制成图象(如图).计算:(1)2g石灰石样品中含杂质______g;
(2)求该石灰石的纯度;
(3)100g这种石灰石与足量的稀盐酸反应,能制取多少克二氧化碳?
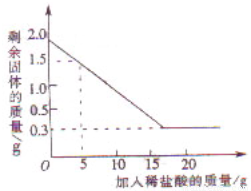
【答案】分析:由于第1、2、3次加入5g稀盐酸时固体的质量都是减少了0.5g,说明5g稀盐酸恰好能够和0.5g碳酸钙完全反应,即5g稀盐酸最多能和0.5g碳酸钙反应,而第4次再加入5g稀盐酸时固体只减少了0.2g,说明固体中的碳酸钙已经全部参与反应,剩余的0.3g固体不能和稀盐酸反应,即石灰石样品中杂质是0.3g,碳酸钙的质量是(2g-0.3g)=1.7g.根据质量分数计算公式便可计算出石灰石的纯度(石灰石中碳酸钙的质量分数).然后根据化学方程式和碳酸钙的质量(石灰石的质量乘以其纯度)就可求出制取的二氧化碳的质量.
解答:解:(1)从图看剩余的0.3g固体不能和稀盐酸反应,即石灰石样品中杂质是0.3g,故答案为:0.3g
(2)石灰石的纯度,即石灰石中碳酸钙的质量分数:
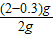 ×100%=85%;
×100%=85%;
(2)设100g这种石灰石与足量的稀盐酸反应,能制取的二氧化碳的质量是x.
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
100g×85% x
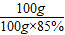 =
=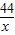
解得:x=37.4g
答:(1)石灰石样品的纯度是85%;
(2)100g这种石灰石与足量的稀盐酸反应,能制取37.4克二氧化碳.
点评:本题难度不是很大,主要考查了如何根据图象去分析数据及根据化学方程式的计算,培养学生分析数据的能力和解决问题的能力.
解答:解:(1)从图看剩余的0.3g固体不能和稀盐酸反应,即石灰石样品中杂质是0.3g,故答案为:0.3g
(2)石灰石的纯度,即石灰石中碳酸钙的质量分数:
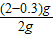 ×100%=85%;
×100%=85%;(2)设100g这种石灰石与足量的稀盐酸反应,能制取的二氧化碳的质量是x.
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
100g×85% x
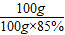 =
=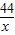
解得:x=37.4g
答:(1)石灰石样品的纯度是85%;
(2)100g这种石灰石与足量的稀盐酸反应,能制取37.4克二氧化碳.
点评:本题难度不是很大,主要考查了如何根据图象去分析数据及根据化学方程式的计算,培养学生分析数据的能力和解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 化学兴趣小组的同学在综合实践中了解到,某石灰厂有一批石灰石原料,其中含有的杂质是二氧化硅(二氧化硅不溶于水,不与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组同学取用2g这种石灰石样品,并取稀盐酸20g分4次加入样品中进行实验,结果如下:
化学兴趣小组的同学在综合实践中了解到,某石灰厂有一批石灰石原料,其中含有的杂质是二氧化硅(二氧化硅不溶于水,不与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组同学取用2g这种石灰石样品,并取稀盐酸20g分4次加入样品中进行实验,结果如下:| 稀盐酸的用量/g | 剩余固体的质量/g |
| 第一次加入5 | 1.5 |
| 第二次加入5 | 1.0 |
| 第三次加入5 | 0.5 |
| 第四次加入5 | 0.3 |
(2)2g此石灰石样品与足量稀盐酸反应最多生成CO2的质量?
 化学兴趣小组同学在综合实践活动中了解到,某石灰厂有一批石灰石原料,其中含有的杂质是二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组同学取用2g这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体的质量见下表,利用实验数据绘制的图象见下图.(保留一位有效数字)
化学兴趣小组同学在综合实践活动中了解到,某石灰厂有一批石灰石原料,其中含有的杂质是二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组同学取用2g这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体的质量见下表,利用实验数据绘制的图象见下图.(保留一位有效数字) 某石灰厂有一批石灰石原料,其中含有的杂质不与盐酸反应.为了测定该石灰石的纯度,兴趣小组的同学取用2g这种石灰石样品,并把20g稀盐酸分四次加入,充分反应后,经过滤、干燥等操作后,根据每次稀盐酸用量及剩余固体质量和实验数据绘制成图象(如图).计算:
某石灰厂有一批石灰石原料,其中含有的杂质不与盐酸反应.为了测定该石灰石的纯度,兴趣小组的同学取用2g这种石灰石样品,并把20g稀盐酸分四次加入,充分反应后,经过滤、干燥等操作后,根据每次稀盐酸用量及剩余固体质量和实验数据绘制成图象(如图).计算: