题目内容
13.构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水.ClO2 是新一代饮用水的消毒剂,我国成功研制出制取ClO2 的新方法,其反应的微观过程图如下:
(其中
 表示氯原子,
表示氯原子, 表示钠原子,
表示钠原子, 表示氧原子)
表示氧原子)试回答:
(1)ClO2 叫做二氧化氯,其中氯元素的化合价为+4;
(2)根据反应的微观过程图写出反应的化学方程式Cl2+2NaClO2=2ClO2+2NaCl.
分析 (1)利用物质的化学式,根据化合物中元素化合价代数和为零,可计算其中氯元素的化合价;
(2)根据反应微观图中各物质的分子构成模型图,判断分子的构成,利用分子构成写出物质的化学式,然后完成反应的化学方程式.
解答 解:(1)ClO2叫做二氧化氯;化学式ClO2中,其中O为-2价,设Cl元素化合价为x,则x+(-2)×2=0,解得x=+4;
(2)该反应的反应物分子为:由每两个氯原子构成的一个氯气Cl2分子,由每一个钠原子、一个氯原子、两个氧原子构成的一个NaClO2分子;生成物的分子为:由每一个氯原子、两个氧原子构成的一个ClO2分子,钠原子和氯原子按照1:1构成的NaCl;观察示意图中各分子的个数比为:1;2:2:2,因此,该反应的化学方程式可写为Cl2+2NaClO2=2ClO2+2NaCl;
故答案为:(1)二氧化氯;+4 (2)Cl2+2NaClO2═2ClO2+2NaCl
点评 本题属于微观示意图的考查,根据构成物质的分子的微观模型图,可判断分子的构成,由分子的构成可确定物质的组成及物质的化学式并书写化学方程式是解题的关键.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
3.谚语诗词中蕴含着科学道理.下列说法正确的是( )
| A. | “真金不怕火炼”是说黄金熔点很高 | |
| B. | “众人拾柴火焰高”是指可燃物越多,着火点越低,越容易着火 | |
| C. | “百炼成钢”与“铁杵磨成针”蕴含的化学原理相同 | |
| D. | “满架蔷薇一院香”的原因是分子在不停地运动 |
4.中学化学中我们学过以下常见的物质:HCl、H2SO4、Ca(OH)2、Na2CO3这四种物质两两间能发生的化学反应共有( )
| A. | 4组 | B. | 5组 | C. | 6组 | D. | 7组 |
1.某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水也不与稀盐酸反应).请计算:
(1)上表中n的数值为4.8.
(2)石灰石中碳酸钙的质量分数为70%.
(3)求盐酸中溶质的质量分数(写出计算过程).
| 序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 第1次 | 20 | 12 |
| 第2次 | 20 | 8 |
| 第3次 | 20 | 4.8 |
| 第4次 | 20 | n |
(2)石灰石中碳酸钙的质量分数为70%.
(3)求盐酸中溶质的质量分数(写出计算过程).
5.选修课上,某化学兴趣小组在老师的帮助下,开展了以下的相关探究:
探究一:氢气的燃烧实验
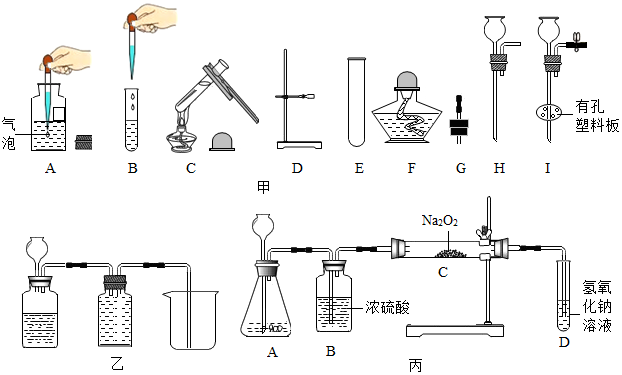
(1)用锌和稀硫酸制取氢气,从图甲中选择仪器组装一套随开随停的发生装置,所需仪器为EI(填编号);反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.
(2)按图乙操作研究氢气的燃烧实验,需用试管收集不同体积比的氢气与空气的混合物,现用(1)中组装的正确装置制取氢气,如何用试管(假设试管容积为10mL)收集氢气与空气体积比为4:1的混合气体,写出其操作方法:试管先装入8mL水,用拇指堵住试管口,倒扣在水槽中,用排水法收集氢气,将剩余的水排出.
(3)用不同体积比的混合气体做氢气的燃烧实验,结果如表:
分析上表信息,你对燃烧或燃烧条件的新认识是燃物能否燃烧除具备燃烧条件,还与可燃物的浓度(或纯度)有关.
探究二:该化学兴趣小组的同学们在一次课外实验中发现一种淡黄色的粉末可以杀菌、消毒和漂白,于是想探究该固体的成分.
提出问题]该淡黄色固体的化学成分是什么?
[查阅资料]
(1)硫单质是一种淡黄色固体,难溶于水.在空气中点燃硫单质,生成一种无色、有刺激性气味的气体.
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热.
[设计实验方案]
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象.
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象.
比较以上两方案,你认为的最佳方案是方案一,理由是(从环保或操作角度分析)操作简单、无污染.
[实验验证并得出结论]
兴趣小组中甲同学向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH).通过实验验证,确定该淡黄色粉末为过氧化钠.甲同学对生成的气体成分判断.他提出了以下三种假设:①该气体是CO②该气体是O2.
你认为上述假设哪个更合理②(填“①”、“②”或“③”);理由是符合质量守恒定律.
[分析]过氧化钠与水反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.
[交流讨论]兴趣小组中乙同学在查阅资料时发现过氧化钠还能与二氧化碳反应,产生一种无色气体.为了验证该结论,该小组同学用图丙所示的装置进行实验,一段实验后,将带火星的木条伸入试管中,发现木条复燃.(温馨提示两点:a.浓硫酸具有吸水性;b.氢氧化钠溶液能与二氧化碳反应.)
B装置能否省去?你的理由是过氧化钠和水反应也会生成氧气;D装置中 的氢氧化钠溶液的作用是防止空气中的二氧化碳与过氧化钠反应.
探究一:氢气的燃烧实验

(1)用锌和稀硫酸制取氢气,从图甲中选择仪器组装一套随开随停的发生装置,所需仪器为EI(填编号);反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.
(2)按图乙操作研究氢气的燃烧实验,需用试管收集不同体积比的氢气与空气的混合物,现用(1)中组装的正确装置制取氢气,如何用试管(假设试管容积为10mL)收集氢气与空气体积比为4:1的混合气体,写出其操作方法:试管先装入8mL水,用拇指堵住试管口,倒扣在水槽中,用排水法收集氢气,将剩余的水排出.
(3)用不同体积比的混合气体做氢气的燃烧实验,结果如表:
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 氢气与空气体积比 | 9:1 | 8:2 | 7:3 | 5:5 | 3:7 | 1:9 | 0.5:9.5 |
| 点燃现象 | 安静 燃烧 | 安静 燃烧 | 弱的 爆鸣声 | 强的 爆鸣声 | 强的 爆鸣声 | 弱的 爆鸣声 | 不燃烧 不爆鸣 |
探究二:该化学兴趣小组的同学们在一次课外实验中发现一种淡黄色的粉末可以杀菌、消毒和漂白,于是想探究该固体的成分.
提出问题]该淡黄色固体的化学成分是什么?
[查阅资料]
(1)硫单质是一种淡黄色固体,难溶于水.在空气中点燃硫单质,生成一种无色、有刺激性气味的气体.
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热.
[设计实验方案]
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象.
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象.
比较以上两方案,你认为的最佳方案是方案一,理由是(从环保或操作角度分析)操作简单、无污染.
[实验验证并得出结论]
兴趣小组中甲同学向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH).通过实验验证,确定该淡黄色粉末为过氧化钠.甲同学对生成的气体成分判断.他提出了以下三种假设:①该气体是CO②该气体是O2.
你认为上述假设哪个更合理②(填“①”、“②”或“③”);理由是符合质量守恒定律.
[分析]过氧化钠与水反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.
[交流讨论]兴趣小组中乙同学在查阅资料时发现过氧化钠还能与二氧化碳反应,产生一种无色气体.为了验证该结论,该小组同学用图丙所示的装置进行实验,一段实验后,将带火星的木条伸入试管中,发现木条复燃.(温馨提示两点:a.浓硫酸具有吸水性;b.氢氧化钠溶液能与二氧化碳反应.)
B装置能否省去?你的理由是过氧化钠和水反应也会生成氧气;D装置中 的氢氧化钠溶液的作用是防止空气中的二氧化碳与过氧化钠反应.
12.现有锌和另外一种金属组成的合金6.5g,向合金中加入一定浓度的100g稀硫酸恰好完全反应,生成氢气Wg,则下列说法正确的是( )
| A. | 若合金是Zn~Al,W可能是0.2g | |
| B. | 若合金是Zn~Fe,则W不可能是0.2g | |
| C. | 若合金是Zn~Cu,W是0.1g,则Zn在混合物中的质量分数为50% | |
| D. | 若合金为Zn~Mg,则加入的稀硫酸的浓度一定大于10% |
9.以下是空气污染指数与质量级别、质量状况的对应关系
垫江县城某日空气污染指数为82~93,根据以上信息,判断当天的空气质量级别和空气质量状况分别是( )
| 空气污染指数 | 0~50 | 51~100 | 101~200 | 201~300 | >300 |
| 空气质量状况 | 优 | 良 | 轻度污染 | 中度污染 | 重度污染 |
| 空气质量级别 | I | II | III | IV | V |
| A. | I级 优 | B. | II级 良 | C. | III级 轻度污染 | D. | V级 重度污染 |
10.高铁酸钾(K2FeO4)是一种高效净水剂,其中Fe的化合价是( )
| A. | +2 | B. | +3 | C. | +6 | D. | -6 |
