题目内容
如图所示是小丽同学配制100g溶质质量分数为12%的NaCl溶液的实验操作示意图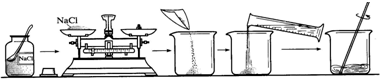
(1)如图中的玻璃仪器分别是广口瓶、量筒、烧杯和
(2)由题意计算:需氯化钠固体 g,水 mL(水的密度是1g/mL),如果现有三种规格的量筒:100mL、50mL、10mL,你认为用哪一种量筒最适宜
(3)配置此溶液的操作步骤: .

(1)如图中的玻璃仪器分别是广口瓶、量筒、烧杯和
(2)由题意计算:需氯化钠固体
(3)配置此溶液的操作步骤:
考点:一定溶质质量分数的溶液的配制,测量容器-量筒
专题:溶液、浊液与溶解度
分析:(1)依据配制溶液的常用仪器回答;
(2)依据溶质的质量=溶液的质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量,结合公式:v=
计算.选择量筒依据‘一次接近’的原则,并结合题意回答;
(3)根据配制溶液的步骤:计算、称量、溶解分析解答;
(2)依据溶质的质量=溶液的质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量,结合公式:v=
| m |
| ρ |
(3)根据配制溶液的步骤:计算、称量、溶解分析解答;
解答:解:(1)图中涉及到的玻璃仪器分别是广口瓶、烧杯、量筒和玻璃棒;
(2)配制100g溶质质量分数为12%的NaCl溶液,需要溶质:100g×12%=12g,水:100g-12g=88g,水的密度是1g/cm3,所以量取的水的体积是88mL,选择100mL的量筒;
(3)配制固体溶质的溶液的步骤是:计算、称量、溶解.
故答案为:(1)玻璃棒;(2)12;88;100mL;(3)计算、称量、溶解.
(2)配制100g溶质质量分数为12%的NaCl溶液,需要溶质:100g×12%=12g,水:100g-12g=88g,水的密度是1g/cm3,所以量取的水的体积是88mL,选择100mL的量筒;
(3)配制固体溶质的溶液的步骤是:计算、称量、溶解.
故答案为:(1)玻璃棒;(2)12;88;100mL;(3)计算、称量、溶解.
点评:熟练掌握配制溶液的步骤,仪器,溶质的质量分数计算是解答此题的基础和关键.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
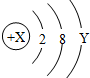 如图是某粒子的结构示意图,回答下列问题:
如图是某粒子的结构示意图,回答下列问题: