题目内容
有一包CuSO4与Na2SO4组成的混合物16.8克,溶于63克水中,然后加入一定量10%的NaOH溶液,恰好完全反应,过滤出9.8克沉淀.求:
(1)原混合物中CuSO4的质量?
(2)加入的NaOH溶液中含有NaOH的质量?
(3)反应后溶液中溶质质量分数?
(1)原混合物中CuSO4的质量?
(2)加入的NaOH溶液中含有NaOH的质量?
(3)反应后溶液中溶质质量分数?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据沉淀的质量利用化学方程式可以求出硫酸铜的质量;
(2)根据沉淀的质量利用化学方程式可以求出氢氧化钠的质量及氢氧化钠溶液的质量;
(3)根据沉淀的质量利用化学方程式可以求出生成的硫酸钠的质量,反应后溶液中溶质为生成的硫酸钠和原混合物中的硫酸钠质量之和,据此解答.
(2)根据沉淀的质量利用化学方程式可以求出氢氧化钠的质量及氢氧化钠溶液的质量;
(3)根据沉淀的质量利用化学方程式可以求出生成的硫酸钠的质量,反应后溶液中溶质为生成的硫酸钠和原混合物中的硫酸钠质量之和,据此解答.
解答:解:设硫酸铜的质量为x,氢氧化钠的质量为y,生成的硫酸钠的质量为z
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160 80 98 142
x y 9.8g z
=
=
=
x=16g,y=8g,z=14.2g
氢氧化钠溶液的质量为:
=80g,
反应后溶液中溶质质量为:16.8g-16g+14.2g=15g,
反应后溶液中溶质质量分数:
×100%=10%
答:(1)原混合物中CuSO4的质量为16g;
(2)加入的NaOH溶液中含有NaOH的质量为8g;
(3)反应后溶液中溶质质量分数为10%.
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160 80 98 142
x y 9.8g z
| 160 |
| x |
| 80 |
| y |
| 98 |
| 9.8g |
| 142 |
| z |
x=16g,y=8g,z=14.2g
氢氧化钠溶液的质量为:
| 8g |
| 10% |
反应后溶液中溶质质量为:16.8g-16g+14.2g=15g,
反应后溶液中溶质质量分数:
| 15g |
| 16.8g+63g+80g-9.8g |
答:(1)原混合物中CuSO4的质量为16g;
(2)加入的NaOH溶液中含有NaOH的质量为8g;
(3)反应后溶液中溶质质量分数为10%.
点评:反应后所得溶液中的溶质为反应生成的和原混合物中存在的.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
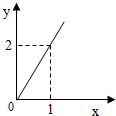 下列不能正确反映对应图象变化关系的纵、横座标的是( )
下列不能正确反映对应图象变化关系的纵、横座标的是( )| A、水中氢元素与氧元素的质量 |
| B、水分子中氢原子与氧原子的个数 |
| C、水电解时生成的氢气与氧气的体积 |
| D、氢气燃烧生成水时消耗的氢气和氧气的体积 |