题目内容
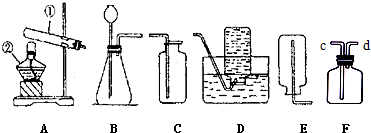
12.通过一年的化学学习,你已经掌握了实验室制取气体的有关规律,请结合下图回答问题: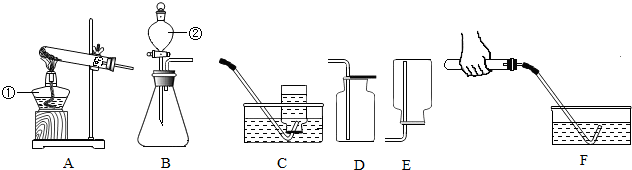
(1)写出图中标号仪器的名称:①酒精灯,②分液漏斗.
(2)实验室中若选择A装置制取氧气.
①反应原理:反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
②实验步骤:
a.按F装置检查装置的气密性,若观察到导管口有气泡冒出,证明装置气密性良好.
b.往试管中装入固体药品,连接并固定好装置.
c.先对试管预热,然后固定在有药品的下方加热,为了收集到比较纯净的氧气,可选用的收集装置为C(选填上图中的标号).
d.用上述方法制取并收集氧气实验结束时,需要进行的操作是先把玻璃导管移出水面
再熄灭酒精灯;待试管冷却后再拆卸装置、洗涤仪器等.
(3)实验室用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是B,若装置内反应剧烈,从实验安全角度考虑,不宜采取的措施有①③(填序号).
①用容积较小的锥形瓶 ②减慢液体的滴加速度
③加热反应物 ④降低液体反应物的浓度.
分析 (1)由仪器的用途和图去分析.
(2)①从A装置的特点是加热固体制取气体,由于试管口有棉花团,故选择的药品为高锰酸钾去分析.
②a.从检查气密性的方法去分析.
c.从用排水法收集氧气更纯去分析;
d.从实验结束,要先把导管移出水面去分析.
(3)从实验室制取二氧化碳气体的药品为大理石和稀盐酸,二者接触就会发生反应,生成氯化钙和水和二氧化碳,由于反应物是固体和液体反应且不需要加热去分析,
①从装置内反应剧烈,产生气体较多,如果用容积较小的锥形瓶会引起爆炸去分析;
②从减慢液体的滴加速度,通过控制液体的量,达到控制反应速率的目的去分析;
③从加热可以加快反应速率去分析;
④从反应物的浓度越大,反应速率越快去分析.
解答 解:(1)由仪器的用途和图可知①为酒精灯,②为分液漏斗;故答案为:酒精灯 分液漏斗.
(2)①A装置的特点是加热固体制取气体,由于试管口有棉花团,故选择的药品为高锰酸钾.用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,所以化学方程式为:2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;故答案为:2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
②a.检查气密性,先把导管浸入水中,用手紧握试管,观察水中的管口有没有气泡冒出;如果有气泡冒出,说明装置不漏气.故答案为:导管口有气泡冒出.
c.用向上排空气法收集时,集气瓶口是一个敞开环境,外面的空气可能进入集气瓶内,而用排水法收集时,由水形成的密闭环境,故收集到的氧气更纯.故答案为:C;
d.实验结束,要先把导管移出水面,如果先停止加热,随着试管温度的降低,试管内气体的体积越来越小,压强也越来越小,外部气压大于试管内气压,在大外部大气压的作用下,水槽内的水倒吸到试管内,引起试管温度骤然降低,导致试管炸裂.故答案为:先把玻璃导管移出水面,再熄灭酒精灯.
(3)实验室制取二氧化碳气体的药品为大理石和稀盐酸,二者接触就会发生反应,生成氯化钙和水和二氧化碳,由于反应物是固体和液体反应且不需要加热,故发生装置为:B,
①装置内反应剧烈,产生气体较多,如果用容积较小的锥形瓶会引起爆炸;故错误;
②减慢液体的滴加速度,通过控制液体的量,达到控制反应速率的目的,故正确;
③加热可以加快反应速率,使反应更加剧烈,容易引起爆炸;故错误;
④反应物的浓度越大,反应速率越快,降低液体反应物的浓度,可以减慢反应速度;故正确;
由于题目要求选出不宜采取的措施;故答案为:①③.
点评 实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度;考查了实验室制取氧气的反应原理,及注意事项,是考试的重点也是中考的重点.

| A. | 用闻气味的方法区别白酒和白醋 | |
| B. | 向洗净的碎鸡蛋壳中加入食盐水可制二氧化碳 | |
| C. | 用肥皂水区别硬水与软水 | |
| D. | 用食醋除水壶中的水垢 |
| 选项 | 物质(杂质) | 除杂质所用试剂或方法 |
| A | NaCl(CaCl2) | 溶解、过滤 |
| B | FeCl2溶液(CuCl2) | 加入过量铁粉、过滤 |
| C | CO2(CO) | 通过灼热的氧化铜 |
| D | 铜(铁) | 用磁铁吸 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 1个-氧化碳分子:Co | B. | 2个亚铁离子:2Fe3+ | ||
| C. | 3个碳酸根离子:3CO32- | D. | 4个氢原子:2H2 |
| A. | 某些非金属氧化物能和碱反应生成盐和水;例如:二氧化碳和三氧化硫 | |
| B. | 一般固体物质的溶解度随温度的升高而增大;例如:氢氧化钙和氯化钠 | |
| C. | 常温下金属一般为固态;例如:汞和金 | |
| D. | 置换反应一定有单质和化合物生成;例如:一氧化碳和氧化铁在高温下反应 |
| A. | 铝合金门窗变旧变暗后可用砂纸或钢丝球打磨变亮 | |
| B. | 废旧金属的回收有利于环境保护并能节约资源和能源 | |
| C. | 合金比纯金属有较大的性质差异,在生活中有更为广泛的用途 | |
| D. | 用钢铁制作的自行车棚应定期喷涂油漆防锈 |
| 物质 | 杂质 | 除去杂质的试剂或方法 | |
| A | NaCl | KNO3 | 溶解、降温结晶、过滤、蒸发结晶 |
| B | CaO | CaCO3 | 适量稀盐酸 |
| C | NaCl溶液 | Na2SO4溶液 | 适量Ba(NO3)2溶液 |
| D | Cu | Fe | CuSO4溶液 |
| A. | A | B. | B | C. | C | D. | D |