题目内容
14.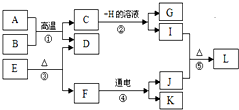 A~L分别为九年级化学学过的不同物质,它们存在右图所示的转化关系.已知A为红棕色固体,B、D均为无色气体,H的溶液呈蓝色.
A~L分别为九年级化学学过的不同物质,它们存在右图所示的转化关系.已知A为红棕色固体,B、D均为无色气体,H的溶液呈蓝色.(1)E的化学式是H2CO3,G的名称为硫酸亚铁.
(2)写出反应①的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)写出反应⑤的化学方程式2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
(4)①~⑤中属于置换反应的有②.
分析 根据A~L分别为九年级化学学过的不同物质,A为铁锈的主要成分,所以A是氧化铁,B、D均为无色气体,A和B高温会生成C和D,所以B是一氧化碳,D是二氧化碳,F通电会生成J和K,所以F是水,J、K是氧气或氢气,E分解水生成水和二氧化碳,所以E是水,H的溶液呈蓝色,所以H可以是硫酸铜,铁和硫酸铜反应生成硫酸亚铁和铜,I会与J反应生成L,所以G是硫酸亚铁,I是铜,J是氧气,K是氢气,L是氧化铜,然后将推出的物质进行验证即可.
解答 解:(1)A~L分别为九年级化学学过的不同物质,A为铁锈的主要成分,所以A是氧化铁,B、D均为无色气体,A和B高温会生成C和D,所以B是一氧化碳,D是二氧化碳,F通电会生成J和K,所以F是水,J、K是氧气或氢气,E分解水生成水和二氧化碳,所以E是H2CO3,H的溶液呈蓝色,所以H可以是硫酸铜,铁和硫酸铜反应生成硫酸亚铁和铜,I会与J反应生成L,所以G是硫酸亚铁,I是铜,J是氧气,K是氢气,L是氧化铜,经过验证,推导正确,所以E的化学式是H2CO3,G的名称为硫酸亚铁;
(2)反应①是一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)反应⑤是氧气和铜在加热的条件下生成氧化铜,化学方程式为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
(4)反应①为氧化铁与一氧化碳反应生成铁和二氧化碳;反应②为铁和硫酸铜反应生成硫酸亚铁和铜,为置换反应;反应③为碳酸分解水生成水和二氧化碳,为分解反应;反应④为水通电生成氢气和氧气,为分解反应;反应⑤为氧气和铜在加热的条件下生成氧化铜,为化合反应,故①~⑤中属于置换反应的有②.
故答案为:
(1)H2CO3,硫酸亚铁;(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(3)2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.(4)②
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 名校课堂系列答案
名校课堂系列答案| A. | 为预防缺碘甲状腺肿大的发生,提倡某些特定人群食用加碘食盐 | |
| B. | 在特制的饭盒夹层中分别装入生石灰和水,食用前使它们混合可以加热食物 | |
| C. | 硫酸铜溶液可以杀菌,所以可用于饮用水消毒 | |
| D. | 在发酵面团中加入适量的碳酸钠揉合,除去面团中多余的酸 |
| A. | 称氯化钠固体时,氯化钠放入左盘 | |
| B. | 用量筒量水时,面对刻度仰视凹液面的最低处读数 | |
| C. | 将量筒内的水倒入烧杯时,有水溅出 | |
| D. | 将配好的溶液倒入细口瓶时,不慎洒落 |
| A. | 红磷在氧气中燃烧发出耀眼的白光,并产生大量的白雾 | |
| B. | 细铁丝在空气中燃烧,火星四射,生成一种黑色固体 | |
| C. | 加热铜绿时,绿色固体变成黑色,管壁出现小水珠 | |
| D. | 某同学在做一氧化碳还原氧化铁的实验过程中,观察到试管中黑色粉末逐渐变红 |
