题目内容
7.钛具有硬度大、密度小、熔点高、抗腐蚀性远优于不锈钢等优良性能,被誉为“未来金属”.地球表面富含钛铁矿石,钛铁矿石的主要成分是FeTiO3.(1)已知FeTiO3中钛的化合价为+4价,则铁的化合价为+2价.
(2)冶炼金属钛时,先将铁铁矿石转化为TiCl4,TiCl4再与Na在一定条件下反应生成Ti和NaCl,请写出后一步反应的化学方程式:TiCl4+4Na═Ti+4NaCl(不要求标出反应条件),其基本反应类型是置换反应.
(3)在冶炼钛的同时,还得到金属铁,请举出铁的一种用途:建造桥梁.
(4)铁比钛易生锈,请写出防止铁生锈的一种方法:涂油漆.
分析 (1)根据化合物中各元素化合价的代数和为零求出铁的化合价;
(2)根据反应物及生成物写出化学方程式,注意配平并根据反应特征确定萁基本反应特征;
(3)钢铁可用于制作机床底座、建造桥梁、修建铁轨等;
(4)从控制铁生锈的条件方面考虑防止铁生锈的方法.
解答 解:(1)设铁元素的化合价为x,根据化合物中各元素化合价的代数和为零的规律,可得x+(+4)+(-2)×3=0;解之得x=+2.
故答案为:+2价.
(2)TiCl4与Na在一定条件下能反应生成Ti和NaCl.用化学方程式表示为:TiCl4+4Na═Ti+4NaCl,从反应前后各物质的种类来看,是一种单质和一种化合物反应生成另一种单质和另一种化合物.符合置换反应的特征.
故答案为:TiCl4+4Na═Ti+4NaCl;置换反应.
(3)钢铁可以制作机床底座、建造桥梁、修建铁轨等.
故答案为:建造桥梁(合理即可);
(4)铁生锈的条件是与空气(氧气)和水分同时接触,要防止铁生锈则是通过控制生锈的条件来实现.一是保持铁制品表面的干燥,二是使铁制品与空气隔绝.常用的方法有涂油、喷漆等.
故答案为:涂油漆(涂油或镀金属等).
点评 本题以一种金属矿物为切入点综合考查了化合价、化学方程式及金属的防锈方面的知识.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | 4个H2O分子和1个H2SO4分子所含氧原子个数相等 | |
| B. | C24H38O4中碳、氧元素质量比为6:1 | |
| C. | 2gH2和32gO2充分反应后生成34gH2O | |
| D. | $\stackrel{+2}{Mg}$:“+2”表示每个镁离子带两个单位正电荷 |
15.从金属材料的发展历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事,这个先后顺序跟什么有关( )
①金属活动性顺序②地壳中金属元素的含量③金属的延展性
④金属的导电性⑤金属的冶炼难易程度.
①金属活动性顺序②地壳中金属元素的含量③金属的延展性
④金属的导电性⑤金属的冶炼难易程度.
| A. | ①④ | B. | ①⑤ | C. | ②③ | D. | ④⑤ |
12. 某气体可能含有水蒸气、CO、H2中的一种或几种.为了确定其成分,最佳的实验方案是将气体依次通过如图的装置( )
某气体可能含有水蒸气、CO、H2中的一种或几种.为了确定其成分,最佳的实验方案是将气体依次通过如图的装置( )
 某气体可能含有水蒸气、CO、H2中的一种或几种.为了确定其成分,最佳的实验方案是将气体依次通过如图的装置( )
某气体可能含有水蒸气、CO、H2中的一种或几种.为了确定其成分,最佳的实验方案是将气体依次通过如图的装置( )| A. | 丙、甲、丙、乙 | B. | 甲、乙、丙 | C. | 丙、甲、乙、丙 | D. | 丙、甲、乙 |

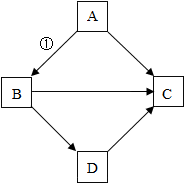 物质之间的相互转化是科学中的重要知识.某同学在复习物质性质时,绘制了如下框图.框图中“→”表示物质之间可以向箭头所指方向一步转化.根据框图,回答下列问题.
物质之间的相互转化是科学中的重要知识.某同学在复习物质性质时,绘制了如下框图.框图中“→”表示物质之间可以向箭头所指方向一步转化.根据框图,回答下列问题.