题目内容
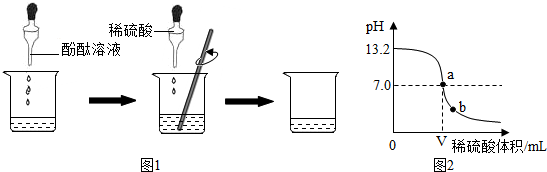
2.下列实验操作错误的是( )
| A. | ①②③ | B. | ①② | C. | ①③④ | D. | ① |
分析 ①根据使用胶头滴管滴加少量液体的方法进行分析判断.
②根据给试管中的液体加热的方法进行分析判断.
③根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断.
④根据向试管中倾倒液体药品的方法进行分析判断.
解答 解:①使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,取液后的胶头滴管不能倒置,以防止污染胶头;图中所示操作错误.
②给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的$\frac{1}{3}$,图中所示操作正确.
③量筒读数时视线要与量筒内液体的凹液面的最低处保持水平,图中所示操作正确.
④向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,图中所示操作正确.
故①实验操作错误.
故选:D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
12.下列生活中常见的变化,一定发生化学变化的是( )
| A. | 食物腐烂 | B. | 冰雪融化 | C. | 玻璃破碎 | D. | 香水扩散 |
13. 2015年3月17日农业部有关负责人表示:到2020年我国化肥利用率达到40%以上,力争实现农作物化肥使用量零增长,某菜农使用的化肥,其包装袋上的部分说明如图所示,下列对该化肥的认识不正确的是( )
2015年3月17日农业部有关负责人表示:到2020年我国化肥利用率达到40%以上,力争实现农作物化肥使用量零增长,某菜农使用的化肥,其包装袋上的部分说明如图所示,下列对该化肥的认识不正确的是( )
 2015年3月17日农业部有关负责人表示:到2020年我国化肥利用率达到40%以上,力争实现农作物化肥使用量零增长,某菜农使用的化肥,其包装袋上的部分说明如图所示,下列对该化肥的认识不正确的是( )
2015年3月17日农业部有关负责人表示:到2020年我国化肥利用率达到40%以上,力争实现农作物化肥使用量零增长,某菜农使用的化肥,其包装袋上的部分说明如图所示,下列对该化肥的认识不正确的是( )| A. | 硝酸铵属于氮肥 | B. | 保存时应注意防潮 | ||
| C. | 含氮量氮元素的质量分数 | D. | 可以与草木灰等碱性物质混合施用 |
17. 化学与健康
化学与健康
“APEC”会议的晚宴上有一道传统小吃“豌豆黄”,根据表格中的信息回答下列问题.
(1 )“豌豆黄”中主要含有蛋白质、糖类和无机盐三类营养素.
(2)“豌豆黄”中含有钙元素.人体缺钙常会引起BD(填字母序号).
A.贫血症 B.佝偻病 C、甲状腺肿大 D、骨质疏松.
 化学与健康
化学与健康“APEC”会议的晚宴上有一道传统小吃“豌豆黄”,根据表格中的信息回答下列问题.
| 品名 | 豌豆黄 |
| 主要原料 | 豌豆 |
| 主要营养成分 | 蛋白质、糖类、钠、钙、钾、镁等元素 |
(2)“豌豆黄”中含有钙元素.人体缺钙常会引起BD(填字母序号).
A.贫血症 B.佝偻病 C、甲状腺肿大 D、骨质疏松.
7. 如图是元素X的一种粒子结构示意图,下列说法正确的是( )
如图是元素X的一种粒子结构示意图,下列说法正确的是( )
 如图是元素X的一种粒子结构示意图,下列说法正确的是( )
如图是元素X的一种粒子结构示意图,下列说法正确的是( )| A. | X是金属元素 | |
| B. | 该粒子可表示为X2- | |
| C. | 该粒子的核电荷数为10 | |
| D. | 该粒子最外层电子层已达到稳定结构 |
14.下列物质中,属于纯净物的是( )
| A. | 煤 | B. | 天然气 | C. | 酒精 | D. | 石油 |
12.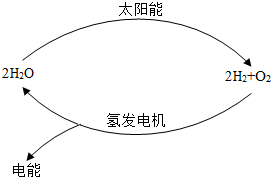 如图是一种最理想的氢能源循环体系,下列说法不正确的是( )
如图是一种最理想的氢能源循环体系,下列说法不正确的是( )
 如图是一种最理想的氢能源循环体系,下列说法不正确的是( )
如图是一种最理想的氢能源循环体系,下列说法不正确的是( )| A. | 该氢能源循环体系能实现将太阳能转化为电能 | |
| B. | 此循环中发生了反应:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | |
| C. | 该过程的实现,将解决能源危机和环境污染问题 | |
| D. | 目前化学家急需解决的问题是寻找合适的光照条件下分解水的催化剂 |