题目内容
12.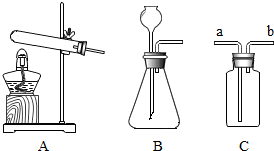 根据如图装置回答下列问题:
根据如图装置回答下列问题:(1)实验室里制取某种气体既可用装置A,也可以用装置B.分别写出用装置A和装置B制取该气体的化学方程式.
(2)若用装置C收集这种气体,应从a(填“a”、“b”)端进气.证明该气体是否收集满的方法是什么?
分析 (1)实验室制取氧气时,可以用加热高锰酸钾或氯酸钾的方法制取,也可以用过氧化氢分解的方法制取;
(2)据氧气的密度比空气大及氧气验满的方法解答.
解答 解:(1)实验室里既可用装置A,也可以用装置B制取的气体是氧气;
用A装置制取氧气时,因为试管口没有塞一团棉花,所以不能用加热高锰酸钾制取,只能够用加热氯酸钾的方法制取,氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气,反应的化学方程式为:
2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2;
用B装置制取氧气的药品是过氧化氢和二氧化锰,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)氧气的密度比空气大,若用装置C收集气体应从a进入,氧气验满的方法法把带火星的木条放在b端验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了.
故答案为:(1)2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)a、带火星的木条放在b端验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了.
点评 选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、密度、能否和空气中的物质发生化学反应等因素.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
2.将下列金属与稀盐酸接触,无气泡产生的是( )
| A. | Fe | B. | Mg | C. | Zn | D. | Cu |
3.发酵粉的主要成分中含有碳酸氢钠.某化学兴趣小组的同学对碳酸氢钠的性质进行了探究.
Ⅰ.定性探究
实验一:探究碳酸氢钠溶液的酸碱性用pH试纸测得碳酸氢钠溶液的pH约为8,可知碳酸氢钠溶液碱性.
实验二:探究碳酸氢钠的热稳定性
【查阅资料]碳酸氢钠受热容易分解,生成水、一种气体和一种常见的固体物质.
【实验1】取一定质量的碳酸氢钠放到铜片上加热,如图所示.

(1)加热一段时间后,观察到烧杯内壁有水珠.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊,说明该气体是CO2.
(3)欲通过进一步的实验探究来确定充分加热后的固体产物的成分.
①可能是Na2CO3 ②可能是NaOH
③可能是NaOH和Na2CO3
【实验2】
【实验结论】NaHCO3受热分解的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
【延伸拓展】实验室有两瓶失去标签的固体药品,已知它们是碳酸钠和碳酸氢钠,你能否设计一个实验进行鉴别,请简述你的实验方案及现象和结论取样,分别放入试管中加热,无明显变化的是碳酸钠,试管壁有水珠且产生的气体能使澄清石灰水变浑浊的是碳酸氢钠.
Ⅱ.定量探究
为测定某发酵粉中碳酸氢钠的质量分数,计了如下实验,其主要实验步骤如下:

①按如图组装仪器,取50g品放入锥形瓶中,关闭塞b,打开活塞a,从导管A处缓缓鼓入一定量的空气;
②关闭活塞a,打开活塞b,加入足量稀硫酸溶液,直至锥形瓶内不再产生气泡;
③关闭活塞b,打开活塞a,从导管A处缓缓鼓入一定量的空气;
④测量干燥管内碱石灰(氧化钙和氢氧化钠固体的混合物)增加的质量(见下图曲线);
⑤重复步骤③和④的操作,直至干燥管内物质质量不再增加.
(1)步骤①加入样品前还应检查装置的气密性.
(2)装置甲的作用是吸收空气中的二氧化碳,装置乙的作用是吸收水分;
(3)请利用相关数据计算样品中碳酸氢钠的质量分数.(写出计算过程)
Ⅰ.定性探究
实验一:探究碳酸氢钠溶液的酸碱性用pH试纸测得碳酸氢钠溶液的pH约为8,可知碳酸氢钠溶液碱性.
实验二:探究碳酸氢钠的热稳定性
【查阅资料]碳酸氢钠受热容易分解,生成水、一种气体和一种常见的固体物质.
【实验1】取一定质量的碳酸氢钠放到铜片上加热,如图所示.

(1)加热一段时间后,观察到烧杯内壁有水珠.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊,说明该气体是CO2.
(3)欲通过进一步的实验探究来确定充分加热后的固体产物的成分.
①可能是Na2CO3 ②可能是NaOH
③可能是NaOH和Na2CO3
【实验2】
| 实验操作 | 实验现象 | 实验结论 |
| A.将该固体溶于蒸馏水配制成溶液,取少量溶液于试 管中,滴加足量稀盐酸 | 有气体产生 | 假设 ②(填序号)不成立 |
| B.另取少量溶液于试管中,滴加 足量BaCl2溶液 | 产生白色沉淀 | 固体产物中有 Na2CO3 |
| C.取上述B步骤静置后所得上层清液,滴入少量 无色酚酞溶液 | 无明显现象 | 假设①成立 |
【延伸拓展】实验室有两瓶失去标签的固体药品,已知它们是碳酸钠和碳酸氢钠,你能否设计一个实验进行鉴别,请简述你的实验方案及现象和结论取样,分别放入试管中加热,无明显变化的是碳酸钠,试管壁有水珠且产生的气体能使澄清石灰水变浑浊的是碳酸氢钠.
Ⅱ.定量探究
为测定某发酵粉中碳酸氢钠的质量分数,计了如下实验,其主要实验步骤如下:

①按如图组装仪器,取50g品放入锥形瓶中,关闭塞b,打开活塞a,从导管A处缓缓鼓入一定量的空气;
②关闭活塞a,打开活塞b,加入足量稀硫酸溶液,直至锥形瓶内不再产生气泡;
③关闭活塞b,打开活塞a,从导管A处缓缓鼓入一定量的空气;
④测量干燥管内碱石灰(氧化钙和氢氧化钠固体的混合物)增加的质量(见下图曲线);
⑤重复步骤③和④的操作,直至干燥管内物质质量不再增加.
(1)步骤①加入样品前还应检查装置的气密性.
(2)装置甲的作用是吸收空气中的二氧化碳,装置乙的作用是吸收水分;
(3)请利用相关数据计算样品中碳酸氢钠的质量分数.(写出计算过程)
20.下列各项中,前者一定大于后者的是( )
| A. | 20℃时KNO3的溶解度、80℃时KNO3的溶解度 | |
| B. | NaNO3不饱和溶液的质量分数、NaNO3饱和溶液的质量分数 | |
| C. | NH4NO3溶于水后溶液的温度、NaOH溶于水后溶液的温度 | |
| D. | 10g铝与足量盐酸反应生成H2的质量、10g镁与足量盐酸反应生成H2的质量 |
7.下列实验现象的描述中,正确的是( )
| A. | 硫粉在空气中燃烧,火焰为蓝紫色,放出大量的热,生成二氧化碳 | |
| B. | 将铝丝插入硫酸铜溶液中,溶液由蓝色变为浅绿色 | |
| C. | 将氢氧化钠溶液滴入氯化铁溶液中,有红褐色沉淀产生 | |
| D. | 将二氧化碳通入紫色石蕊溶液中,溶液变为蓝色 |
17.今年“两会”议政,环保清单中“低碳生活、减排治霾”仍为一大主题,下列不属于空气污染物的是( )
| A. | CO | B. | NO2 | C. | CO2 | D. | SO2 |
4.下列溶液中,能使酚酞溶液变红的是( )
| A. | 烧碱溶液 | B. | 稀硫酸 | C. | 稀盐酸 | D. | 食盐水 |
11.央视新闻频道曾播出《每周质量报告》3•15特别行动-《“健美猪”真相》,曝光河南省孟州市等地养猪场采用违禁动物药品“瘦肉精”饲养生猪.“瘦肉精”是一类药物,它是能够抑制肥肉、促进瘦肉生长的药物添加剂,食用对人体产生危害,长期食用则有可能导致染色体畸变,诱发恶性肿瘤.如盐酸莱克多巴胺(化学式:C18H23NO3Cl).下列关于对盐酸莱克多巴胺的说法错误的是( )
| A. | 它的相对分子质量是336.5 | |
| B. | 它是由碳氢氮氧氯五种元素组成的 | |
| C. | 它属于氧化物 | |
| D. | C18H23NO3Cl 分子中碳氢氮氧氯原子个数比为18:23:1:3:1 |