题目内容
20.下列各项中,前者一定大于后者的是( )| A. | 20℃时KNO3的溶解度、80℃时KNO3的溶解度 | |
| B. | NaNO3不饱和溶液的质量分数、NaNO3饱和溶液的质量分数 | |
| C. | NH4NO3溶于水后溶液的温度、NaOH溶于水后溶液的温度 | |
| D. | 10g铝与足量盐酸反应生成H2的质量、10g镁与足量盐酸反应生成H2的质量 |
分析 A、根据硝酸钾的溶解度受温度变化影响进行判断;
B、NaNO3在不同温度下的溶解度是不同的,则其饱和溶液的溶质质量分数也是不同的;
C、根据物质溶解时的吸热或放热现象进行判断;
D、根据选项中元素的相对原子质量和它们与稀盐酸反应的化学方程式,计算出1g这些金属分别与足量稀盐酸反应生成氢气的质量,再进行比较即可.
解答 解:A、硝酸钾的溶解度随着温度的升高而增大,则20℃时KNO3的溶解度小于80℃时KNO3的溶解度,故A错误;
B、没有指明是否是在同一温度下NaNO3的饱和溶液和不饱和溶液,无法比较其溶质质量分数的大小,故B错误;
C、硝酸铵溶于水会吸收大量的热,使溶液的温度降低.NaOH溶于水氢氧化钠溶于水放出大量的热,使溶液的温度升高,则NH4NO3溶于水后溶液的温度小于NaOH溶于水后溶液的温度,故C错误;
D、Mg的相对原子质量为24,24g镁可反应生成2g氢气,即1g镁生成$\frac{1}{12}$克氢气.
Al的相对原子质量为27,27g铝可反应生成3g氢气,即1g铝生成$\frac{1}{9}$克氢气.
故10g铝与足量盐酸反应生成H2的质量大于10g镁与足量盐酸反应生成H2的质量.
故D正确.
故选:D.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
11.“舌尖上的中国”的热播让厨房再次成为人们施展厨艺的舞台,其实厨房也是同学们的家庭实验室,利用厨房中的物品不可以进行的实验是( )
| A. | 探究铁制品在什么条件下生锈 | |
| B. | 探究食盐在水中的溶解能力 | |
| C. | 用燃着的火柴检查天然气管道是否漏气 | |
| D. | 探究鸡蛋壳成分含有碳酸盐 |
8.下列叙述错误的是( )
| A. | 健康饮食强调食用的“绿色食品”,指的是绿颜色的食品 | |
| B. | 篝火晚会时通常把木柴架空一些能使燃烧更旺 | |
| C. | 自行车支架上刷上油漆既美观又能防止钢铁生锈 | |
| D. | 利用洗涤剂的乳化功能可洗去餐具上的油污 |
15.关于玻璃棒在实验中的作用,下列叙述错误的是( )
| A. | 固体溶解时搅拌可以加速溶解 | |
| B. | 测溶液pH时用它蘸取少量溶液 | |
| C. | 过滤时在漏斗中搅拌固液混合物,可以加快过滤速度 | |
| D. | 蒸发液体时搅拌可防止局部温度过高,造成液滴飞溅 |
5.“加强河湖管理,建设生态文明”是2014年我国纪念世界水日和中国水周活动的宣传主题.以下有关水的认识不正确的是( )
| A. | 洗菜的水可以用来浇花 | B. | 肥皂水可鉴别硬水和软水 | ||
| C. | 废水无色透明就可以排入长江 | D. | 水由氢、氧两种元素组成 |
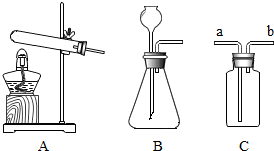 根据如图装置回答下列问题:
根据如图装置回答下列问题: