题目内容
20.为了分析石灰石的纯度,小明同学取石灰石样品25g,加入装有100g稀盐酸的烧杯后恰好完全反应(杂质不参与反应),反应后测得烧杯中物质的总质量为116.2g.试计算:(1)生成二氧化碳的质量是多少?这些二氧化碳在标准状况下的体积是多少?(标准状况下二氧化碳的密度是1.977g/L)
(2)该石灰石的纯度是多少?
分析 分析所发生的反应,可发现反应后总质量减轻是由于生成了气体二氧化碳,因此,可知恰好完全反应时放出二氧化碳的质量为8.8g;然后利用二氧化碳的质量,根据反应的化学方程式,分别计算恰好完全反应时碳酸钙的质量,最后使用质量分数的计算公式,求出样品中碳酸钙的质量分数.
解答 解:(1)依据质量守恒定律可知,生成二氧化碳的质量为:100g+25g-116.2g=8.8g,
体积为:$\frac{8.8g}{1.977g/L}$=4.45L;
(2)样品中CaCO3的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
x 8.8 g
$\frac{100}{x}$=$\frac{44}{8.8g}$
x=20g
样品中碳酸钙的质量分数为:$\frac{20g}{25g}$×100%=80%.
故答案为:(1)8.8g,4/45L;
(2)80%.
点评 根据化学方程式进行计算时,只能使用纯净物的质量进行计算,而不能把混合物的质量直接代入化学方程式进行计算.

练习册系列答案
相关题目
10.规范实验操作是实验成功的基础和关键.下列实验基本操作正确的是( )
| A. |  稀释浓硫酸 稀释浓硫酸 | B. |  称11.5g氯化钠 | C. |  滴加液体 | D. |  收集氧气 |
11.检验一瓶长期暴露在空气中氢氧化钠是否变质,下列可作为检验试剂的是( )
| A. | 稀盐酸 | B. | 无色酚酞 | C. | 紫色石蕊试液 | D. | 水 |
8.氢氧化钠与酸、二氧化碳反应没有明显现象.小军和小晴两位同学想用实验证明氢氧化钠能与盐酸、二氧化碳反应,他们做了以下探究过程.
【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳.
【设计实验】小军设计了两个实验进行验证,请你帮他完成如表实验报告.
【反思交流】小晴认为:小军设计的上述两个实验都有缺陷,不足以证明氢氧化钠能与盐酸和二氧化碳反应.请您分析:
(1)小军的第一个实验的缺陷是用过量的盐酸,应改为适量的盐酸.
(2)小晴用上述小军第二个实验的装置和药品,验证氢氧化钠可以与二氧化碳反应,她的设计方案是:分别量取40mLNaOH和Ca(OH)2溶液放A、B中,关闭K时,B中溶液无明显变化,且通入的二氧化碳体积远大于A中溶液的体积,此实验可以说明氢氧化钠和二氧化碳发生了反应..
【实验结论】通过小晴的实验,证明了氢氧化钠可以与盐酸和二氧化碳反应.因此您认为小军的实验方案②中,装置B中无现象出现最主要的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示)
【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳.
【设计实验】小军设计了两个实验进行验证,请你帮他完成如表实验报告.
| 实验操作 | 实验现象 | 实验结论及解释 | |
| ① | 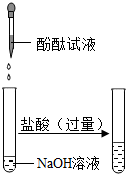 | 酚酞试液滴入氢氧化钠中变红色,滴入过量盐酸酚酞试液又变无色 | 氢氧化钠可以与盐酸反应. 该反应的化学方程式为: NaOH+HCl=NaCl+H2O |
| ② | 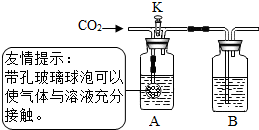 小军选用NaOH和Ca(OH)2两种溶液分别放入上边装置中的广口瓶中,关闭K,通入二氧化碳. | A、B中均无明显变化. | B中盛放的溶液是氢氧化钙. 该实验目的是 氢氧化钠可以与二氧化碳反应. |
(1)小军的第一个实验的缺陷是用过量的盐酸,应改为适量的盐酸.
(2)小晴用上述小军第二个实验的装置和药品,验证氢氧化钠可以与二氧化碳反应,她的设计方案是:分别量取40mLNaOH和Ca(OH)2溶液放A、B中,关闭K时,B中溶液无明显变化,且通入的二氧化碳体积远大于A中溶液的体积,此实验可以说明氢氧化钠和二氧化碳发生了反应..
【实验结论】通过小晴的实验,证明了氢氧化钠可以与盐酸和二氧化碳反应.因此您认为小军的实验方案②中,装置B中无现象出现最主要的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示)
5.下列实验现象的描述错误的是( )
| A. | 硫在空气中燃烧,发出淡蓝色火焰,生成有刺激性气味的气体 | |
| B. | 木炭在氧气中燃烧发出白光 | |
| C. | 白磷自燃时,产生大量白雾 | |
| D. | 镁带在空气中燃烧发出耀眼白光,生成白色固体 |
12.下列各组物质的溶液,只需用稀硫酸就能鉴别出来的是( )
| A. | NaOH、NaCl、Na2CO3 | B. | Na2CO3、Ba(NO3)2、KOH | ||
| C. | Ba(OH)2、NaNO3、KCl | D. | K2CO3、Ba(NO3)2、BaCl2 |
9.甲同学做铁在氧气中燃烧实验时,先在集气瓶中放了少量水;乙同学做硫在氧气中燃烧实验时,仿照甲同学的操作,也在集气瓶中放少量水(其中溶有氢氧化钠),请简要说明上述两个实验放少量水作用是否相同,为什么?
18.在“2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑”的化学反应过程中,保持不变的粒子是( )
| A. | H2O | B. | H2 | C. | O2 | D. | H和O |