题目内容
15.归纳总结是学习科学的重要方法,顾远同学用图甲总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).
(l)在图甲中,顾远同学还有一条关于NaOH的化学性质未总结,请你帮它在④(非金属氧化物)处总结好.
(2)顾远同学还采用微观示意图乙来说明反应②的发生,从该图可以看出,反应前后没有发生变化的微观粒子有Na+、S${{O}_{4}}^{2-}$.(写离子符号)
(3)为了验证反应①能够发生,顾远选择下列哪种物质D.
A.HNO3 B.NaCl C.Na2CO3 D.CuSO4.
分析 (1)根据碱的化学性质进行分析;
(2)根据氢氧化钠和硫酸反应生成硫酸钠和水进行分析;
(3)根据复分解反应发生的条件进行分析.
解答 解:(1)氢氧化钠除了能够和酸碱指示剂、酸、某些盐溶液反应外,还能够和二氧化碳等非金属氧化物反应,因此④处是非金属氧化物;
(2)氢氧化钠和硫酸反应生成硫酸钠和水,所以从该图可以看出,反应前后没有发生变化的微观粒子有:Na+、S${{O}_{4}}^{2-}$;
(3)反应①是碱和盐的反应,而A是酸,Na2CO3、CuSO4、NaCl都是盐,但这三中盐中只有硫酸铜能和氢氧化钠反应生成硫酸钠和氢氧化铜沉淀,符合复分解反应发生的条件,故选:D.
故答案为:(1)④非金属氧化物;
(2)Na+、S${{O}_{4}}^{2-}$;
(3)D.
点评 本题考查了常见的碱的化学性质及复分解反应发生的条件,属于基础性的考查,难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
5. 下列表中各物质不能按照图中关系(“→”表示反应一步完成)转化的是( )
下列表中各物质不能按照图中关系(“→”表示反应一步完成)转化的是( )
 下列表中各物质不能按照图中关系(“→”表示反应一步完成)转化的是( )
下列表中各物质不能按照图中关系(“→”表示反应一步完成)转化的是( )| 物质选项 | A | B | C | D |
| X | BaCl2 | Na2SO4 | Cu | CaO |
| Y | Ba(NO3)2 | NaCl | CuO | CaCl2 |
| Z | BaCO3 | NaNO3 | CuSO4 | CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
7.实验室常用酸化的碘化钾(KI)和淀粉检验碘酸钾(KIO3).下列有关说法正确的是( )
| A. | KI和KIO3都属于酸 | |
| B. | KIO3中碘元素的化合价为+5 | |
| C. | 碘元素在KI和KIO3中的质量分数相等 | |
| D. | 淀粉遇到碘元素变蓝色 |
4.下列各物质中,括号内为杂质,除去杂质的方法正确的是( )
| 物质及杂质 | 除杂方法 | |
| A | MnO2(KClO3) | 加热 |
| B | CO2(CO) | 通入O2并点燃 |
| C | KNO3溶液(CuSO4) | 加入适量的氢氧化钡溶液并过滤 |
| D | FeCl3溶液(KCl) | 加入适量的氢氧化钾溶液、过滤再向滤出固体中加入适量稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
5.钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与如图2.请根据有关信息回答问题.
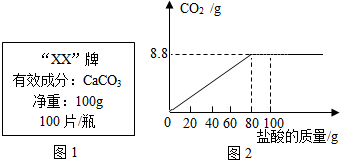
(1)人体缺钙易出现的疾病是骨质疏松,a的数值为25
(2)求品牌补钙药剂中CaCO3的质量分数.
(3)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).

| 第1次 | 第3次 | 第4次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | a | 20 |
(2)求品牌补钙药剂中CaCO3的质量分数.
(3)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).