题目内容
2.某同学设计了下面五个实验,能够借助托盘天平直接验证质量守恒定律的实验共有( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
分析 做验证质量守恒定律的实验时选用药品和装置应该考虑到:①只有质量没有变化的化学变化才能验证质量守恒;②如果反应物中有气体参加反应,或生成物中有气体生成,设计验证质量守恒定律的实验,最好在密闭容器中.
解答 解:实验甲中,酒精与水混合后并没有发生化学反应,不能验证质量守恒定律;
实验乙中,铁和硫酸铜反应生成铜和硫酸亚铁,没有物质跑出来,反应前后容器中物质的总质量也不变,故能够借助托盘天平直接验证质量守恒定律;
实验丙中,由于采用的是敞口容器,稀盐酸与碳酸钠反应后生成的CO2气体逸散到空气中,使得生成物质量减小,不能直接验证质量守恒定律.
实验丁中,采用的是密闭容器,白磷燃烧生成五氧化二磷,没有物质跑出来,反应前后容器中物质的总质量也不变,故能够借助托盘天平直接验证质量守恒定律;
实验戊中,空气中的氧气参加反应,不能直接验证质量守恒定律.
故选B.
点评 通过回答本题要知道在设计验证质量守恒定律的实验时最好在密闭容器中进行,不允许有任何物质跑掉.

练习册系列答案
相关题目
10.要想从食盐溶液中得到食盐晶体,宜采取的方法是( )
| A. | 蒸发溶剂的方法 | B. | 冷却热饱和溶液的方法 | ||
| C. | 倒掉部分溶液的方法 | D. | 升高温度的方法 |
17.下列说法正确的是( )
| A. | 均一、稳定的液体都是溶液 | |
| B. | 碘酒具有消毒杀菌的作用,是一种溶液,其中溶剂是水,溶质是碘 | |
| C. | 20℃时,10g水中最多可以溶解3.6g食盐,所以食盐属于易溶物质 | |
| D. | 25℃时,向100g质量分数为10%的氯化钠溶液中加入10g蔗糖粉末,完全溶解后,溶液中氯化钠的质量分数将不变 |
7.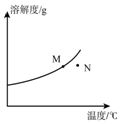 如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
 如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )| A. | 从N→M:先向N中加入适量固体A再降温 | |
| B. | 从N→M:先将N降温再加入适量固体A | |
| C. | 从M→N:先将M降温过滤后再将其升温 | |
| D. | 从M→N:先将M升温再将其蒸发掉部分水 |
14.下列对化学反应类型的判断,错误的是( )
| A. | 2H2S+SO2═3S↓+2H2O (复分解反应) | |
| B. | CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO (化合反应) | |
| C. | 2AgBr$\stackrel{光照}{→}$2Ag+Br2↑ (分解反应) | |
| D. | 2Mg+CO2$\frac{\underline{\;高温\;}}{\;}$2MgO+C (置换反应) |
12.下列图象能正确反映所对应叙述关系的是( )
| A. |  向 pH=3 的溶液中不断加水 | |
| B. |  一定量的稀硫酸与锌粒反应 | |
| C. |  向 H2SO4 和 CuSO4 混合液中加 NaOH 溶液 | |
| D. |  给氯酸钾和二氧化锰的混合物加热 |


 把一个小铃通过细线固定在盛满SO2的集气瓶中,向瓶中倒入NaOH溶液,迅速塞紧并轻轻振荡,过一会儿,再摇动集气瓶,只看到小铃的振动,却听不到铃声.试运用所学的科学知识进行解释.
把一个小铃通过细线固定在盛满SO2的集气瓶中,向瓶中倒入NaOH溶液,迅速塞紧并轻轻振荡,过一会儿,再摇动集气瓶,只看到小铃的振动,却听不到铃声.试运用所学的科学知识进行解释. 敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质,请写出此过程的化学方程式:,现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并震荡.如图表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况.那么,图线BC段对应的实验现象是有气泡生成,在C点时溶液中的溶质是NaCl.
敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质,请写出此过程的化学方程式:,现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并震荡.如图表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况.那么,图线BC段对应的实验现象是有气泡生成,在C点时溶液中的溶质是NaCl.