题目内容
6.硬水中含有较多的可溶性钙、镁化学物,硬水会给生活和生产带来很多麻烦.(1)硬水可用来肥皂水区分,生活中可以用加热煮沸的方法来降低水的硬度
(2)硬水在加热或久置时,会产生水垢(主要成分是Mg(OH)2和CaCO3,生活中可以用适量的稀盐酸除去水瓶上的水垢,写出相关反应中属于中和反应的方程式:Mg(OH)2+2HCl═MgCl2+2H2O.
分析 (1)根据硬水与软水的检验方法、转化方法进行分析解答.
(2)根据水垢的主要成分、酸的化学性质进行分析,写出反应的化学方程式即可.
解答 解:(1)硬水和软水的区别在于所含的钙镁离子的多少,生活中可用肥皂水来区分硬水和软水,产生泡沫较多的是软水,较少的硬水.生活中常用煮沸的方法来降低水的硬度.
(2)水垢的主要成分是Mg(OH)2和CaCO3,均能与稀盐酸反应;Mg(OH)2和稀盐酸反应生成氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O;碳酸钙与稀盐酸反应生成氯化钙、水、二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.其中属于中和反应是Mg(OH)2+2HCl=MgCl2+2H2O.
故答案为:(1)肥皂水;煮沸.
(2)Mg(OH)2+2HCl═MgCl2+2H2O.
点评 本题难度不大,掌握硬水与软水的检验方法、转化方法、酸的化学性质、化学方程式的书写方法等即可正确解答本题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.用排空气法收集H2、O2或CO2,利用如图装置可以收集的气体是( )


| A. | 只有H2 | B. | 只有H2和CO2 | C. | 只有O2和CO2 | D. | H2、O2、CO2都可以 |
17.下列图象能正确反映实验过程中相应量变化的是( )
| A. |  将不饱和硝酸钾溶液缓慢降温 | |
| B. | 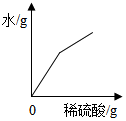 向一定量的氢氧化钠溶液中加过量稀硫酸 | |
| C. |  向氢氧化钠溶液中加水 | |
| D. | 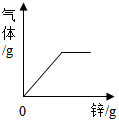 向一定量的稀硫酸中加入过量的锌 |
1.某元素X(不是稀有气体)的原子最外层有2个电子,而Y原子的最外电层有7个电子.则这两种元素组成的化合物的化学式为( )
| A. | X2Y7 | B. | X7Y2 | C. | X2Y | D. | XY2 |
11.下列操作方法错误的是( )
| 选项 | 实验目的 | 操作 |
| A | 除去硝酸钾中混有的少量氯化钠 | 用降温结晶的方法提纯硝酸钾 |
| B | 鉴别硝酸铵、硫酸铜、碳酸钙 | 分别取样,加适量水观察现象 |
| C | 分离氯化钾和二氧化锰的混合物 | 溶解、过滤、洗涤、蒸发结晶 |
| D | 稀释浓硫酸 | 将浓硫酸沿容器壁缓缓倒入水中并不断搅拌 |
| A. | A | B. | B | C. | C | D. | D |
18.配制50g溶质的质量分数为2%的氯化钠溶液,不需要的仪器是( )
| A. | 漏斗 | B. | 玻璃棒 | C. | 烧杯 | D. | 量筒 |
15.铝制品中日常生活中应用广泛,但铝制品却不宜长时间盛放腌制食品.资料显示:“铝制品表面虽然有一层致密的氧化膜保护…氯化钠也会破坏氧化膜的结构,加速铝制品的腐蚀.”(氯化钠中水的作用下会解离出阴阳离子:NaCl═Na++Cl-)
【提出问题】氯化钠溶液中的哪一种离子对氧化膜产生了破坏作用?
【实验方案】
【提出问题】氯化钠溶液中的哪一种离子对氧化膜产生了破坏作用?
【实验方案】
| 序号 | 实验1 | 实验2 | 实验3 |
实 验 方 案 | 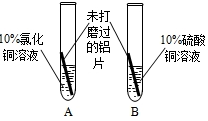 | 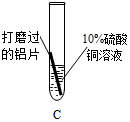 |  |
| 现 象 | A中铝片表面有红色固体析出;B中铝片无明显现象 | 铝片表面有红色固体析出,溶液由蓝色逐渐变为无色 | 与A中的现象相同 |
结 论 | 溶液中对氧化膜产生了破坏作用的离子可能是氯离子. | 除去表面氧化膜的铝会与CuSO4溶液反应.该反应的化学方程式为 2Al+3CuSO4═Al2(SO4)3+3Cu. | 验证了实验1的结论 |